Získávání energeticky významných prvků z oceánů (II): Vodík
Postupně docházející zásoby fosilních paliv by bez nalezení efektivního zástupného zdroje energie mohly vyvolat energetickou krizi. Vodík by se měl po vyčerpání těchto tradičních surovin stát plnohodnotnou a ekologickou náhradou.
Objev vodíku a jeho izotopy
Vodík je nejjednodušší a nejlehčí prvek. Vyskytuje se ve všem živém, v každé kapce vody a život bez něj tudíž nemůže existovat. Ve své čisté formě je bezbarvý, bez chuti, bez zápachu a netoxický. Zatímco v atmosféře se prakticky nevyskytuje, je nejhojněji zastoupeným prvkem ve vesmíru. Můžeme jej nalézt na Slunci a dalších hvězdách, kde je hlavním zdrojem energie pro fúzní reakce. Ačkoliv byl vyroben mnohem dříve, identifikován byl ve směsi hořlavých plynů až v roce 1766 britským vědcem Henrym Cavendishem. Jméno mu dal v roce 1783 Lavoisier. Izotopy vodíku byly objeveny až ve 20. století. Deutérium objevila skupina amerických vědců vedená Haroldem Ureyem v roce 1932. Konečně tritium vyrobila v roce 1935 další skupina amerických vědců, vedená Rutherfordem.
Vodík jako palivo
Mnoha lidem se zdá vodík jako nové palivo, ale ve skutečnosti jsme jej využívali tisíce let ve formě fosilních paliv. Velké množství energie obsažené ve fosilních palivech pochází z vodíkových vazeb a interakcí v jejich chemické struktuře. Benzín může být ukázkovým příkladem výnosného fosilního paliva, protože obsahuje velké množství energie zhuštěné a svázané v malém objemu. Z toho plyne praktická využitelnost benzínu v automobilovém průmyslu, kde je skladní prostor velice důležitý. Nicméně toto využití má nepříznivý ekologický dopad, protože spalováním benzínu vzniká velké množství škodlivých látek.
Nejefektivnějším využitím vodíku jako paliva je jeho aplikace v čisté formě uvolňováním zásobní energie buď spalováním nebo elektrochemickou reakcí. Jeho spalování je poměrně neškodné a produkuje pouze vodu, teplo a malé množství oxidu dusného jako vedlejšího produktu. Nicméně spalování není příliš efektivní metodou, protože množství energie uvolněné při spalování je ve formě tepla, které není užitečné pro pohon automobilů.
Mnohem efektivnější cestou jak získávat energii z vodíku je elektrochemická reakce v palivovém článku. Reakcí vodíku s kyslíkem v palivovém článku vzniká energie ve formě elektřiny. Tato elektřina může být využita na pohon automobilů, letadel, jako zdroj tepla aj. Navíc pokud palivový článek pracuje při vysokých teplotách, může být systém nastaven jako kogenerační jednotka a využívat odpadní energii jako zdroj tepla. Výhodou výroby energie touto cestou je, že jedinými vedlejšími produkty jsou teplo a vodní pára a nejsou produkovány žádné skleníkové plyny anebo jiné ekologicky závadné odpadní produkty. Pro pohon elektrolyzéru může být využita obnovitelná energie - větrná, vodní, sluneční, přílivová, tudíž lze zabezpečit bezemisní výrobu energie.
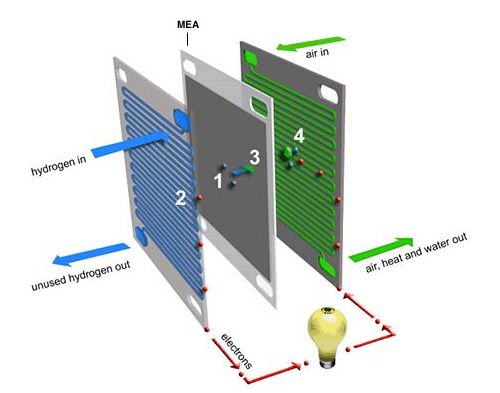
Palivový článek s protonovou membránou
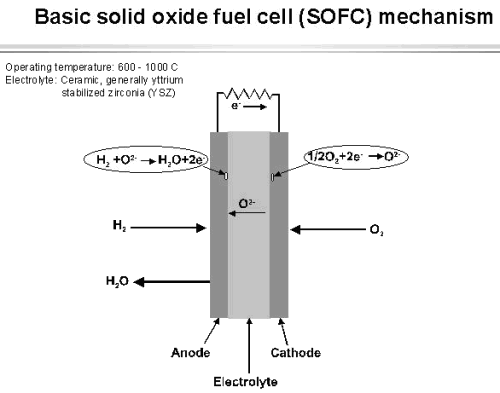
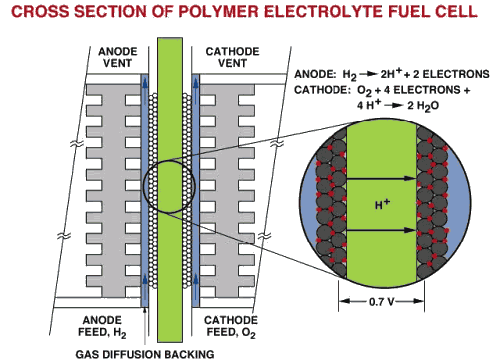
Polymerní elektrolytický palivový článek
Výroba vodíku
Ačkoliv se vodík vyskytuje téměř ve všech věcech, jež nás obklopují, málokdy jej můžeme najít v čisté formě. Nejčastěji je svázán s jinými atomy ve sloučeninách jako zemní plyn a voda. Z nich musí být nejprve izolován přidáním energie nutné k rozbití vazeb mezi atomy. Ať už je to metan, zemní plyn, uhlí, biomasa nebo voda, tak každá technologie výroby přináší jistá rizika, různé množství vynaložené energie a různé množství odpadních látek. V současné době se vyrábí zhruba 95 % vodíku ze zemního plynu, který je tvořen uhlovodíky. Vodík se z nich izoluje katalytickou reakcí s vodní parou. Nicméně zásoby zemního plynu postupně docházejí a výrobní proces není z nejekologičtějších, protože produkuje skleníkové plyny. Proto průmyslová výroba vodíku ze zemního plynu nemá široké uplatnění ve vzdálenější budoucnosti. Dalším způsobem výroby vodíku je elektrolýza vody. Na elektrolýzu však musíme další energii dodat, abychom vodík získali. Proto v tomto procesu není vodík zdrojem energie, ale jen jejím nositelem.
Výroba vodíku ve velkém má i své proti
Matematické modely studií budoucího hromadného využití vodíku simulují nebezpečí, které může způsobit vodík unikající do atmosféry. Jeho hromadění ve stratosféře může napomáhat vzniku ozónové díry. Unikající vodík stoupá do stratosféry, kde z něho reakcí s hydroxylovými radikály (skupina OH-) vzniká voda. Plyn tak napomáhá vzniku chladné a dlouhodobě přetrvávající oblačnosti v oblasti pólů. Riziko jinak čistého a zdánlivě neškodného slučování spočívá v tom, že vytváří příznivé podmínky pro následné reakce halogenů, jako je chlór. Ty ničí atmosférický ozón a zpomalují obnovu ozónové vrstvy. Není to ovšem jediné riziko. Uniklý vodík také zvyšuje koncentrace skleníkových plynů v atmosféře. Opět to souvisí se zánikem radikálů OH-, ale tentokrát v troposféře. Skupina OH- k sobě váže veškeré znečišťující látky včetně metanu, jednoho z nejzávažnějších skleníkových plynů. Snížené hladiny OH- tak umožňují metanu přetrvávat v ovzduší delší dobu.
Trocha čísel o vodíku
Cena energie z obnovitelných zdrojů klesá stejným tempem, jako roste cena energie získaná z fosilních zdrojů. Např. v roce 1999 stál 1 kg vodíku získaný ze zemního plynu okolo 65 centů, cena benzínu byla nižší než 1 USD/gallon (asi 3,8 l) a cena energie získaná z větrné elektrárny byla 10 centů za 1 kWh. V srpnu 2005 stojí 1 kg vodíku získaný ze zemního plynu okolo 1,2 USD, cena benzínu se pohybuje okolo 2,3 USD/gallon a cena energie získaná z větrné elektrárny je okolo 4 centů za 1 kWh.
Pro srovnání, účinnost přenosu energie na pohon kol u benzínem poháněných strojů je okolo 14 %, u hybridních aut okolo 26 % a u aut poháněných palivovými články okolo 42 %.
 Honda FCX - auto na palivový článek |
 Doplňování energie u Hondy FCX |
Uskladňování vodíku
Uskladňování vodíku stlačením je podobné jako např. u zemního plynu. Nejčastěji se vodík uskladňuje pod tlakem 20-25 MPa ve válcových nádobách o objemu nad 50 litrů. Chceme-li uskladnit větší množství, používají se pracovní tlaky 50-60 MPa, ačkoliv největší zásobníky na světě (okolo 15.000 m3) pracují při tlacích 12-15 MPa. Kvůli snížení objemu uskladňovaného vodíku se provádí jeho zkapalňování. Pro zkapalnění je nutné vodík přivést k teplotám okolo -250 °C, což je energeticky poměrně nákladné. Výhodou zkapalnění vodíku je množství energie, kterou z daného objemu získáme (je cca 3x vyšší než ze stejného objemu benzínu). Asi nejbezpečnější a nejúčinnější metodou uskladňování vodíku je jeho navázání do chemické struktury látek. Pro tento účel se používají hydridy (např.: LaNi5 nebo FeTi). Například LaNi5 může absorbovat až 7 molů vodíku na 1 mol LaNi5 při normální teplotě a tlaku 253 kPa (do 1 kg lze absorbovat 32,6 g - 362 litrů plynného vodíku - 3,16 hmotnostních %). Hustota rozpuštěného vodíku je dvojnásobná než v samotném zkapalněném plynu a hustota uložené energie je asi 35krát větší než v klasickém olověném akumulátoru. Absorpce vodíku při tvorbě hydridu lze zjednodušit do pěti základních kroků:
- fyzikální sorpce molekul vodíku
- disociace molekul vodíku a začátek chemisorpce
- penetrace povrchu vodíkových atomů
- difúze molekul vodíku vrstvou hydridu
- tvorba hydridu na rozhraní kov/hydrid
Desorpce poté probíhá v podstatě obráceným mechanismem, kdy prvním krokem je rozrušení rozhraní mezi hydridem a kovem.
Jako zásobní látky pro zdroj vodíku lze použít i některé uhlovodíky jako např. metanol nebo cyklohexan. Budoucnost uskladňování vodíku patří zřejmě nanotechnologiím. Běžné hydridy jsou schopny adsorbovat mezi 2-4 hmotnostních procent vodíku, zatímco nanotechnologie předpokládají uskladnit okolo 70 hmotnostních procent.
 Elektrolytická jednotka v Oceánografickém Institutu v Imari |
 Uskladňovací jednotka v Oceánografickém Institutu v Imari |

Pohled na polymerní elektrolytický palivový článek v Oceánografickém Institutu v Imari
Výroba vodíku s pomocí energie získané z oceánu
Hlavním cílem našeho výzkumného centra je ověřit myšlenku získávání energie z oceánů a aplikovat ji v praxi. Pro maličké rovníkové tichomořské ostrůvky (např. Palau, Cookovy nebo Marshallovy ostrovy, Kiribati, Tonga, Tuvalu atd.), které nemají žádné vlastní zdroje fosilních paliv, by bylo vybudování takového systému velmi důležité, protože jim umožní spolehlivě pokrýt veškerou poptávku po elektrické energii. Dalším významným prvkem pro vybudování systému může být výroba, na těchto ostrovech zpravidla nedostatkové, kvalitní minerální pitné vody na desalinační jednotce. Jak elektřina (zejména pro pohon elektrolyzéru), tak voda (z desalinační jednotky) jsou pak posléze primárními zdroji pro provoz jednotky na výrobu vodíku. Vyrobený vodík lze uskladnit ve formě hydridů a využít např. pro pohon automobilů. Studená (hlubokomořská) voda a teplá (povrchová) voda může sloužit na chlazení, resp. ohřívání pracovních jednotek na výrobu vodíku.
Elektrolytická jednotka na výrobu vodíku je schopna vyrobit 1 Nm3 vodíku za hodinu a v současné době pracuje s účinností okolo 90 %. Protože je systém prozatím v testovacím provozu, využívá klasický zdroj energie a i pro elektrolýzu je používaná destilovaná voda. Pro uskladnění vyrobeného vodíku jsou dva kontejnery na hydridy na 10 Nm3, resp. 1 Nm3. Vedle nejběžnějšího hydridu LaNi5 se testuje ještě hydrid s pracovním názvem TL-492 (Mm(La0,6-0,8)Ni4,0Co0,6Mn0,2Al0,2). Je sledována reakční kinetika, v závislosti na teplotě (10-80 °C) a tlaku (0-2 MPa). Grafy adsorpce a desorpce pro oba hydridy jsou uvedeny dále. První výsledky ukazují na efektivnější uskladňování při nízkých teplotách pro LaNi5 a při vyšších teplotách pro TL-492.
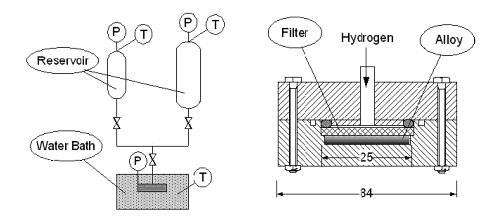
Schéma technologického uspořádání
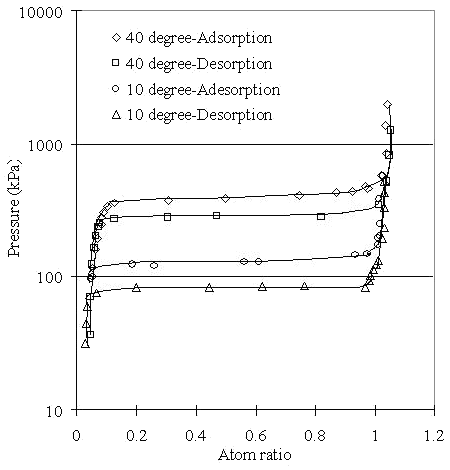
PCT relationship LaNi5
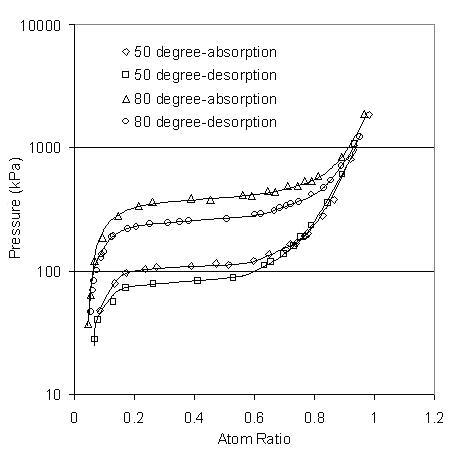
PCT relationship TL-492
Seznam použité literatury:
- Martin M., Gommel C., Borkhart C. and Fromm E.: Absorption and desorption kinetics of hydrogen storage alloys, Journal of Alloys and Compounds 238 (1996), pp. 193-201.
- Wallace W.E., Karlicek R.F. Jr. and Imamura H.: Mechanism of Hydrogen Absorption by LaNi5, The Journal of Physical Chemistry 83 (13), 1979, pp. 1708 - 1712.
- Bae S. Ch., Yang Y., Ikegami Y. and Monde M.: Hydriding and dehydriding reactions of Mm(La0.6-0.8)Ni4.0Co0.6Mn0.2Al0.2 and LaNi5, 8th Asian hydrogen energy conference, (2005), Beijing, China.
- Mintz H. M. and Zeiri Y., Hydriding kinetics of powders, Journal of Alloys and Compounds 216, (1994), pp. 159-175.
- www.enviweb.cz
- www.h2eco.org
- tonto.eia.doe.gov
- www.e-sources.com
- www.generalhydrogen.com
- www.gorvin.mysteria.cz