Nařízení č. 181/2001 Sb. kterým se stanoví technické požadavky na zdravotnické prostředky
PŘEDPIS BYL ZRUŠEN 01.05.2004
| se změnami: | 336/2001 Sb. |
| uveřejněno v: | č. 69/2001 Sbírky zákonů na straně 3810 |
| schváleno: | 25.04.2001 |
| účinnost od: | 08.06.2001 |
| zrušeno: | 01.05.2004 |
| [Textová verze] |
181/2001 Sb.
NAŘÍZENÍ VLÁDY
ze dne 25. dubna 2001,
kterým se stanoví technické požadavky
na zdravotnické prostředky
Změna: 336/2001 Sb.
Vláda nařizuje podle § 22 zákona č. 22/1997 Sb.,
o technických požadavcích na výrobky a o změně a doplnění
některých zákonů, ve znění zákona č. 71/2000 Sb., (dále jen
"zákon") k provedení § 11 odst. 2, § 12 odst. 1 a 4 a § 13 odst.
2 a 4 zákona a k provedení zákona č. 123/2000 Sb.,
o zdravotnických prostředcích a o změně některých souvisejících
zákonů, (dále jen "zákon o zdravotnických prostředcích"):
Úvodní ustanovení
§ 1
Tímto nařízením se v souladu s právem Evropských
společenství1) a s mezinárodní smlouvou2) stanoví technické
požadavky na zdravotnické prostředky.3)
------------------------------------------------------------------
1) Směrnice Rady 93/42/EHS z 14. června 1993 týkající se
zdravotnických prostředků, ve znění směrnice Rady 98/79/ES
z 27. října 1998.
2) Protokol k Evropské dohodě zakládající přidružení mezi Českou
republikou na jedné straně a Evropskými společenstvími a jejich
členskými státy na straně druhé o posuzování shody a akceptaci
průmyslových výrobků.
3) § 2 zákona č. 123/2000 Sb., o zdravotnických prostředcích
a o změně souvisejících zákonů.
§ 2
(1) Stanovenými výrobky podle § 12 odst. 1 zákona jsou pro
účely posuzování shody podle tohoto nařízení zdravotnické
prostředky3) s výjimkou
a) diagnostických zdravotnických prostředků in vitro,4) a
b) aktivních implantabilních zdravotnických prostředků vymezených
v § 2 odst. 2 písm. f) zákona o zdravotnických prostředcích.
(2) Toto nařízení se dále nevztahuje na
a) léčiva,5)
b) kosmetické přípravky,
c) výrobky, které v době jejich uvedení na trh6) obsahují lidskou
krev, výrobky z lidské krve, lidské plazmy nebo krevní buňky
lidského organismu,
d) transplantáty, tkáně nebo buňky lidského organismu a výrobky je
obsahující nebo z nich odvozené,
e) transplantáty, tkáně nebo buňky zvířecího původu, s výjimkou
zdravotnických prostředků vyrobených s využitím neživé či mrtvé
zvířecí tkáně nebo neživých výrobků ze zvířecí tkáně
odvozených, a
f) osobní ochranné prostředky, na které se vztahuje zvláštní
právní předpis.7)
------------------------------------------------------------------
3) § 2 zákona č. 123/2000 Sb., o zdravotnických prostředcích
a o změně souvisejících zákonů.
4) § 2 odst. 2 písm. c) zákona č. 123/2000 Sb.
5) § 2 odst. 1 zákona č. 79/1997 Sb., o léčivech a o změnách
a doplnění některých souvisejících zákonů, ve znění zákona č.
149/2000 Sb.
6) § 3 písm. f) zákona č. 123/2000 Sb.
7) Nařízení vlády č. 172/1997 Sb., kterým se stanoví technické
požadavky na osobní ochranné prostředky, ve znění nařízení
vlády č. 284/2000 Sb.
§ 3
Obecné zásady
(1) Zdravotnický prostředek musí vyhovovat základním
požadavkům uvedeným v příloze č. I k tomuto nařízení (dále jen
"základní požadavky") s přihlédnutím k určenému účelu použití;
základní požadavky se považují rovněž za splněné, jestliže
zdravotnické prostředky odpovídají příslušným harmonizovaným
normám.8)
(2) Pro účely tohoto nařízení se za harmonizované normy8)
považují též články Evropského lékopisu obsahující technické
požadavky týkající se zdravotnických prostředků, zejména
chirurgického šicího materiálu a vzájemného působení léčiv
a materiálu, z něhož byly vyrobeny zdravotnické prostředky, pokud
odkazy na tyto články byly oznámeny v Úředním věstníku Evropského
společenství.
(3) Na trh mohou být zdravotnické prostředky uvedeny, pokud
splňují základní požadavky a další ustanovení tohoto nařízení,
která se na ně vztahují. Do provozu mohou být zdravotnické
prostředky uvedeny pouze tehdy, jestliže splňují podmínky pro
uvedení na trh a byly dodány a instalovány odpovídajícím způsobem
v souladu s určeným účelem použití. Uvedením do provozu se rozumí
okamžik, ve kterém je zdravotnický prostředek připravený poprvé
k určenému účelu použití předán uživateli.
(4) Zdravotnické prostředky uvedené na trh a do provozu
musí být udržovány a používány v souladu s určeným účelem použití.
(5) Zdravotnické prostředky pro klinické zkoušky9) mohou
být za tímto účelem předávány lékařům a jiným osobám, které jsou
na základě své kvalifikace oprávněné provádět klinické zkoušky,
popřípadě klinické hodnocení bez klinických zkoušek za podmínek
stanovených v zákoně o zdravotnických prostředcích,10) v § 15
tohoto nařízení, v příloze č. XVII k tomuto nařízení a v příloze
č. XIV nebo XV k tomuto nařízení.
(6) Zakázkové zdravotnické prostředky11) mohou být uváděny
na trh a do provozu, jestliže u nich byla posouzena shoda
v souladu s
a) § 8 a ve shodě s přílohou č. XIV, nebo
b) § 9 a ve shodě s přílohou č. XV
k tomuto nařízení; zakázkové zdravotnické prostředky tříd IIa, IIb
a III musí mít prohlášení podle přílohy č. XIV k tomuto nařízení.
(7) V případech, kdy zdravotnické prostředky nejsou
v souladu s tímto nařízením a ohrožují zdraví nebo životy lidí
nebo pokud zdravotnické prostředky nesou označení CE12) a jsou
řádně uvedené na trh nebo do provozu anebo zdravotnické prostředky
uvedené v odstavci 6 řádně uvedené do provozu, udržované
a používané v souladu s určeným účelem použití, a přesto existuje
nebezpečí, že mohou negativně ovlivnit zdraví lidí, se zřetelem na
povahu rizika pro uživatele, se postupuje podle zákona, zákona
o zdravotnických prostředcích a podle zvláštního právního
předpisu.13) Jde zejména o případy, jestliže nesoulad
zdravotnického prostředku s tímto nařízením vyplývá z
a) nedodržení základních požadavků,
b) nesprávného použití norem, pokud se prohlašuje, že byly
použity, nebo
c) nedostatku v samotných normách.
(8) Zdravotnické prostředky mohou být uvedeny na trh
v České republice pouze tehdy, jestliže informace o jejich použití
v souladu s přílohou č. I bodem 13 tohoto nařízení jsou uvedeny
v českém jazyce.
(9) Zdravotnické prostředky využívající jadernou energii
nebo zdroje ionizujícího záření musí být posouzeny z hlediska
radiační ochrany osobou s odpovídající akreditací14) pro tuto
činnost.
------------------------------------------------------------------
8) § 4a odst. 1 zákona č. 22/1997 Sb., o technických požadavcích
na výrobky a o změně a doplnění některých zákonů, ve znění
zákona č. 71/2000 Sb.
9) § 2 odst. 2 písm. e) zákona č. 123/2000 Sb.
10) § 8 až 16 zákona č. 123/2000 Sb.
11) § 2 odst. 2 písm. d) zákona č. 123/2000 Sb.
12) Nařízení vlády č. 291/2000 Sb., kterým se stanoví grafická
podoba označení CE, jeho provedení a umístění na výrobku.
13) Zákon č. 64/1986 Sb., o České obchodní inspekci, ve znění
pozdějších předpisů.
14) § 14 zákona č. 22/1997 Sb., ve znění zákona č. 71/2000 Sb.
§ 4
Označování zdravotnických prostředků
(1) Zdravotnický prostředek, který není zakázkový ani určen
pro klinické zkoušky, může být před uvedením na trh a do provozu
označen výrobcem nebo dovozcem českou značkou shody (dále jen
"CCZ"),15) jestliže
a) splnění základních požadavků u tohoto prostředku,
s přihlédnutím k jeho určenému účelu použití, bylo ověřeno
posouzením shody některým z postupů uvedených v § 8, a
b) bylo vydáno prohlášení o shodě.
(2) Výrobce umístí na zdravotnický prostředek, který není
zakázkový ani určen pro klinické zkoušky, nebo na jeho obal před
jeho uvedením na trh a do provozu namísto postupu podle odstavce
1 označení CE,12) jestliže
a) splnění základních požadavků u tohoto prostředku,
s přihlédnutím k jeho určenému účelu použití, bylo ověřeno
posouzením shody některým z postupů uvedených v § 9,
b) bylo vydáno ES prohlášení o shodě, a
c) zdravotnický prostředek má původ v České republice nebo ve
státech, se kterými je sjednána mezinárodní smlouva.2)
(3) Pokud zdravotnický prostředek podléhá z jiných hledisek
i jiným nařízením vlády, které předpokládají označení CCZ nebo
označení CE, pak toto označení vyjadřuje, že zdravotnický
prostředek vyhovuje i těmto jiným nařízením vlády. Výčet
ustanovení použitých nařízení vlády musí být uveden v dokumentech,
upozorněních nebo v návodech, které doprovázejí zdravotnický
prostředek v souladu s tímto nařízením.
(4) Označení CCZ nebo označení CE musí být umístěno
viditelně, čitelně a nesmazatelně na zdravotnickém prostředku nebo
jeho sterilním obalu, pokud je to proveditelné a vhodné, a dále
v návodu na použití. Pokud je to možné, musí být označení CCZ nebo
označení CE i na obalu zdravotnického prostředku, ve kterém se
prodává.
(5) K označení
a) CCZ musí být připojeno, s výjimkou zdravotnických prostředků
třídy I, které nejsou sterilní ani s měřicí funkcí,
identifikační číslo autorizované osoby, která u zdravotnického
prostředku posoudila shodu některým z postupů uvedených
v přílohách č. II, VI, VIII a X k tomuto nařízení,
b) CE musí být připojeno, s výjimkou zdravotnických prostředků
třídy I, které nejsou sterilní ani s měřicí funkcí,
identifikační číslo autorizované osoby, která u zdravotnického
prostředku posoudila shodu některým z postupů uvedených
v přílohách č. III, VII, IX a XI k tomuto nařízení.
(6) Na zdravotnickém prostředku nesmějí být umístěny značky
a popisy, které by omylem mohly být považovány za znaky významem
nebo graficky se podobající označení CCZ nebo označení CE. Jiný
znak lze umístit na zdravotnický prostředek, jeho obal nebo
v návodu doprovázejícím zdravotnický prostředek za předpokladu, že
jím není snížena viditelnost ani čitelnost označení CCZ nebo
označení CE.
(7) Jestliže se pro účely předvádění zdravotnických
prostředků na výstavách, veletrzích i jinak použijí zdravotnické
prostředky, které neodpovídají požadavkům tohoto nařízení, musí
být tyto prostředky viditelně označeny tak, aby bylo patrné, že
nemohou být uváděny na trh a do provozu.
------------------------------------------------------------------
2) Protokol k Evropské dohodě zakládající přidružení mezi Českou
republikou na jedné straně a Evropskými společenstvími a jejich
členskými státy na straně druhé o posuzování shody a akceptaci
průmyslových výrobků.
12) Nařízení vlády č. 291/2000 Sb., kterým se stanoví grafická
podoba označení CE, jeho provedení a umístění na výrobku.
15) Nařízení vlády č. 179/1997 Sb., kterým se stanoví grafická
podoba české značky shody, její provedení a umístění na
výrobku.
§ 5
Neoprávněné připojení označení CCZ nebo označení CE
(1) Jestliže vznikne důvodné podezření, že označení CCZ
nebo označení CE bylo ke zdravotnickému prostředku připojeno
neoprávněně, může být podle zvláštního právního předpisu16)
požádána autorizovaná osoba o účast při posouzení dotčeného
zdravotnického prostředku. Potvrdí-li se podezření podle věty
prvé,
a) výrobce nebo dovozce, anebo
b) výrobce nebo jeho zplnomocněný zástupce
odstraní protiprávní stav podle pokynu České obchodní inspekce.
(2) Zplnomocněným zástupcem podle odstavce 1 písm. b) se
pro účely tohoto nařízení rozumí fyzická osoba s trvalým pobytem
nebo místem podnikání nebo právnická osoba se sídlem ve státech
Evropských společenství, která je písemně pověřena výrobcem
k jednání za něho s úřady a orgány ve státech Evropských
společenství, se zřetelem na požadavky vyplývající pro výrobce
z tohoto nařízení.
(3) Jestliže
a) výrobce nebo dovozce nesplní podmínky pro označení CCZ, nebo
b) výrobce nebo dovozce nesplní podmínky pro označení CE, anebo
c) výrobce nebo jeho zplnomocněný zástupce nesplní podmínky pro
označení CE
a pokyny České obchodní inspekce týkající se zdravotnického
prostředku dotčeného podle odstavce 1, postupuje se podle
zvláštních právních předpisů.17)
(4) O opatřeních podle odstavců 1 a 2 musí být informována
Evropská komise a příslušné orgány členských států Evropských
společenství.
------------------------------------------------------------------
16) § 6 odst. 1 zákona č. 64/1986 Sb., ve znění pozdějších předpisů.
17) § 19 odst. 1 zákona č. 22/1997 Sb., ve znění zákona č.
71/2000 Sb.
§ 7a odst. 1 zákona č. 64/1986 Sb., ve znění zákona č.
240/1992 Sb.
§ 6
Klasifikace
Zdravotnické prostředky se zařazují podle míry rizika,
kterou představuje jejich použití pro uživatele,18) popřípadě pro
jinou fyzickou osobu, do tříd I, IIa, IIb a III; zařazování
zdravotnického prostředku do některé z těchto tříd provádí výrobce
nebo dovozce podle pravidel uvedených v příloze č. XVI k tomuto
nařízení.
------------------------------------------------------------------
18) § 3 písm. e) zákona č. 123/2000 Sb.
Postupy posuzování shody
§ 7
(1) Výrobce nebo dovozce provádí nebo zajišťuje
u zdravotnického prostředku posouzení shody postupy a úkony, které
jsou uvedeny v § 8 až 11.
(2) Jestliže výrobce nebo dovozce zamýšlí umístit na
zdravotnický prostředek označení CCZ nebo jej uvést na trh v České
republice bez tohoto označení, použije některý z postupů
posuzování shody uvedený v § 8 a přílohách č. II, IV, VI, VIII, X
a XII k tomuto nařízení.
(3) Jestliže výrobce zamýšlí opatřit zdravotnický
prostředek označením CE, použije některý z doporučených postupů
posuzování shody uvedený v § 9 a přílohách č. III, V, VII, IX, XI
a XIII k tomuto nařízení.
(4) Na pokyn výrobce je zplnomocněný zástupce oprávněn
zahájit postup podle příloh uvedených v odstavci 3.
§ 8
(1) U zdravotnického prostředku třídy III, který není
zakázkový ani určený pro klinické hodnocení, výrobce nebo dovozce
postupuje při
a) posouzení systému jakosti autorizovanou osobou podle přílohy č.
II k tomuto nařízení, nebo
b) přezkoušení typu zdravotnického prostředku autorizovanou osobou
podle přílohy č. IV k tomuto nařízení s
1. ověřením shody zdravotnického prostředku s jeho
certifikovaným typem na každém zdravotnickém prostředku nebo
statisticky vybraném vzorku autorizovanou osobou podle
přílohy č. VI k tomuto nařízení, nebo
2. posouzením systému jakosti výroby podle přílohy č. VIII
k tomuto nařízení.
(2) U zdravotnického prostředku třídy IIa, který není
zakázkový ani určený pro klinické zkoušky, výrobce nebo dovozce
postupuje při posuzování shody podle přílohy č. XII k tomuto
nařízení s
a) ověřením shody na každém zdravotnickém prostředku nebo
statisticky vybraném vzorku, a to autorizovanou osobou podle
přílohy č. VI k tomuto nařízení, nebo
b) posouzením systému jakosti výroby podle přílohy č. VIII
k tomuto nařízení, nebo
c) posouzením systému jakosti zdravotnických prostředků podle
přílohy č. X k tomuto nařízení,
nebo podle odstavce 3 písm. a).
(3) U zdravotnického prostředku třídy IIb, který není
zakázkový ani určený pro klinické zkoušky, výrobce nebo dovozce
postupuje při
a) posouzení systému jakosti autorizovanou osobou podle přílohy č.
II k tomuto nařízení s výjimkou bodu 4 této přílohy, nebo
b) přezkoušení typu zdravotnického prostředku autorizovanou osobou
podle přílohy č. IV k tomuto nařízení s
1. ověřením shody zdravotnického prostředku s jeho
certifikovaným typem na každém zdravotnickém prostředku nebo
statisticky vybraném vzorku autorizovanou osobou podle
přílohy č. VI k tomuto nařízení, nebo
2. posouzením systému jakosti výroby podle přílohy č. VIII
k tomuto nařízení, nebo
3. posouzením systému jakosti zdravotnických prostředků podle
přílohy č. X k tomuto nařízení.
(4) U zdravotnického prostředku třídy I, s výjimkou
zakázkového zdravotnického prostředku nebo zdravotnického
prostředku určeného pro klinické zkoušky, výrobce nebo dovozce
před jeho uvedením na trh postupuje při posuzování shody podle
přílohy č. XII k tomuto nařízení a § 14.
(5) Při zpracování prohlášení o shodě u
a) zakázkového zdravotnického prostředku postupuje výrobce nebo
dovozce před jejich uvedením na trh podle přílohy č. XIV
k tomuto nařízení,
b) ostatních zdravotnických prostředků postupuje výrobce nebo
dovozce před jejich uvedením na trh podle § 14.
§ 9
(1) U zdravotnického prostředku třídy III, který není
zakázkový ani určený pro klinické zkoušky, se výrobce při
připojování označení CE řídí postupem podle
a) ES prohlašování shody podle přílohy č. III (Systém úplného
zabezpečení jakosti) k tomuto nařízení, nebo
b) ES přezkoušení typu podle přílohy č. V k tomuto nařízení ve
spojení s postupem pro
1. ES ověřování podle přílohy č. VII k tomuto nařízení, nebo
2. ES prohlašování shody podle přílohy č. IX (Zabezpečení
jakosti výroby) k tomuto nařízení.
(2) U zdravotnického prostředku třídy IIa, který není
zakázkový ani určený pro klinické zkoušky, se výrobce při
připojování označení CE řídí postupem pro ES prohlašování o shodě
podle přílohy č. XIII k tomuto nařízení ve spojení s postupem pro
a) ES ověřování podle přílohy č. VII k tomuto nařízení, nebo
b) ES prohlašování shody podle přílohy č. IX (Zabezpečení jakosti
výroby) k tomuto nařízení, nebo
c) ES prohlašování shody podle přílohy č. XI (Zabezpečení jakosti
zdravotnického prostředku) k tomuto nařízení,
nebo podle odstavce 3 písm. a).
(3) U zdravotnického prostředku třídy IIb, který není
zakázkový ani určený pro klinické zkoušky, se výrobce při
připojování označení CE řídí postupem pro
a) ES prohlašování shody podle přílohy č. III (Systém úplného
zabezpečení jakosti) k tomuto nařízení s výjimkou bodu 4 této
přílohy, nebo
b) ES přezkoušení typu podle přílohy č. V k tomuto nařízení ve
spojení s postupem pro
1. ES ověřování podle přílohy č. VII k tomuto nařízení,
2. ES prohlašování shody podle přílohy č. IX (Zabezpečení
jakosti výroby) k tomuto nařízení, nebo
3. ES prohlašování shody podle přílohy č. XI (Zabezpečení
jakosti zdravotnického prostředku) k tomuto nařízení.
(4) U zdravotnického prostředku třídy I, který není
zakázkový ani určený pro klinické zkoušky, se výrobce při
připojování označení CE řídí postupem podle přílohy č. XIII
k tomuto nařízení a vypracuje ES prohlášení o shodě před uvedením
tohoto zdravotnického prostředku na trh.
(5) Před uvedením každého zakázkového zdravotnického
prostředku na trh výrobce postupuje podle přílohy č. XV k tomuto
nařízení a vypracuje prohlášení stanovené touto přílohou. Výrobce
předá České obchodní inspekci i Státnímu ústavu pro kontrolu léčiv
(dále jen "ústav") na jejich vyžádání seznam zakázkových
zdravotnických prostředků, které byly uvedeny do provozu v České
republice.
§ 10
(1) Při posuzování shody u zdravotnického prostředku
výrobce, popřípadě autorizovaná osoba zohledňuje výsledky
hodnocení a ověřovacích postupů, pokud byly provedeny v souladu
s tímto nařízením v jednotlivých mezistupních výrobního procesu.
(2) Jestliže postup posuzování shody u zdravotnického
prostředku zahrnuje účast autorizované osoby,
a) výrobce nebo dovozce, anebo
b) výrobce nebo jeho zplnomocněný zástupce
požádá o tuto službu podle svého výběru autorizovanou osobu
s odpovídajícím rozsahem autorizace.
(3) Autorizovaná osoba může požadovat nezbytně nutné
informace pro ověření shody z hlediska zvoleného postupu
posuzování shody.
(4) Rozhodnutí autorizované osoby učiněná v souladu
s přílohami č. II a IV nebo III a V k tomuto nařízení jsou platná
po dobu nejdéle 5 let a mohou být prodloužena o dalších 5 let,
a to na základě žádosti výrobce podané v době uvedené ve smlouvě
mezi výrobcem a autorizovanou osobou, která rozhodnutí učinila.
(5) Průvodní a výrobní dokumentaci zdravotnického
prostředku, záznamy a korespondenci týkající se postupů uvedených
v § 8 a 9 lze pořizovat v úředním jazyce členského státu, ve
kterém jsou postupy prováděny, popřípadě v jiném jazyce, který je
pro autorizovanou osobu přijatelný.
§ 11
Zvláštní postup posuzování shody pro systémy a soupravy
zdravotnických prostředků a jejich sterilizace
(1) U systémů a souprav zdravotnických prostředků se
postupuje odchylně od § 8 až 10.
(2) Osoba, která sestavuje zdravotnické prostředky označené
CCZ v rámci určených účelů použití sestavených zdravotnických
prostředků, aby je uvedla na trh jako systém nebo soupravu,
vypracuje prohlášení, ve kterém uvede, že
a) ověřila vzájemnou kompatibilitu sestavených zdravotnických
prostředků podle pokynů jejich výrobců a zajistila jejich
provoz v souladu s těmito pokyny,
b) zabalila systém nebo soupravu zdravotnických prostředků
a připojila k ní odpovídající informace pro uživatele včetně
pokynů od výrobců jednotlivých zdravotnických prostředků, a
c) její činnost při sestavování zdravotnických prostředků odpovídá
příslušným metodám vnitřních kontrol a inspekcí.
(3) Osoba, která sestavuje zdravotnické prostředky označené
označením CE v rámci určených účelů použití sestavených
zdravotnických prostředků, aby je uvedla na trh jako systém nebo
soupravu, postupuje obdobně podle odstavce 2.
(4) Nejsou-li splněny podmínky uvedené v odstavcích 2 a 3,
zejména nejsou-li zdravotnické prostředky tvořící systém nebo
soupravu zdravotnických prostředků označeny CCZ nebo označením CE
nebo není-li systém či souprava zdravotnických prostředků
kompatibilní z hlediska původních určených účelů použití
jednotlivých zdravotnických prostředků, považuje se takový systém
nebo souprava zdravotnických prostředků za samostatný zdravotnický
prostředek, na který se vztahuje postup podle § 8 až 10.
(5) Osoba, která za účelem uvedení na trh sterilizuje
systémy nebo soupravy zdravotnických prostředků uvedené
v odstavcích 2 a 3 nebo jiné zdravotnické prostředky označené
a) CCZ, určené jejich výrobci nebo dovozci ke sterilizaci před
jejich použitím v rámci poskytování zdravotní péče, zvolí jeden
z postupů uvedených v přílohách č. VI, VIII nebo X k tomuto
nařízení, anebo
b) označením CE, určené jejich výrobci ke sterilizaci před jejich
použitím v rámci poskytování zdravotní péče, zvolí jeden
z postupů uvedených v přílohách č. VII, IX nebo v příloze č. XI
k tomuto nařízení.
Použití uvedených příloh a činnost autorizované osoby se omezují
na hlediska postupu k dosažení sterility. Osoba uvedená
v předchozí větě vypracuje prohlášení, že sterilizace byla
provedena v souladu s pokyny výrobce nebo dovozce.
(6) Jednotlivé zdravotnické prostředky uvedené v odstavcích
2, 3, 4 a 5 nesmí být dodatečně označeny
a) CCZ, musí však být opatřeny informací podle bodu 13 přílohy č.
I k tomuto nařízení, která obsahuje údaje výrobců nebo dovozců
zdravotnických prostředků, které byly sestaveny, nebo
b) označením CE, musí však být opatřeny informací podle bodu 13
přílohy č. I k tomuto nařízení, která obsahuje údaje výrobců
zdravotnických prostředků, které byly sestaveny.
Prohlášení podle odstavců 2, 3, 4 a 5 uchovává osoba uvedená
v předchozích odstavcích po dobu 5 let od uvedení posledního
systému nebo soupravy zdravotnických prostředků na trh pro potřebu
příslušných úřadů státní správy.
§ 12
Registrace osob zodpovědných za uvádění
zdravotnických prostředků na trh
(1) Výrobce nebo dovozce, který v souladu s postupy podle
§ 8 odst. 4 a 5 uvádí pod svým vlastním jménem zdravotnické
prostředky na trh v České republice, a osoba, která se podílí na
činnostech uvedených v § 11, informuje Ministerstvo zdravotnictví
(dále jen "ministerstvo") v souladu se zákonem o zdravotnických
prostředcích19) o adrese sídla nebo místa podnikání, jde-li
o právnickou osobu, nebo o adrese místa podnikání a trvalého
pobytu, jde-li o fyzickou osobu, a současně sděluje i popis
příslušných zdravotnických prostředků.
(2) Výrobce, který v souladu s postupy podle § 9 odst.
4 a 5 uvádí zdravotnické prostředky na trh ve státech Evropských
společenství, a osoba, která se podílí na činnostech uvedených
v § 11, informuje příslušné úřady členského státu Evropských
společenství, ve kterém má zapsané své sídlo nebo místo podnikání,
o adrese tohoto sídla nebo místa podnikání, jde-li o právnickou
osobu, nebo o adrese místa podnikání a trvalého pobytu, jde-li
o fyzickou osobu, a současně sděluje i popis příslušných
zdravotnických prostředků; v České republice výrobci informují
ministerstvo v souladu se zákonem o zdravotnických
prostředcích.19)
(3) U zdravotnických prostředků tříd IIb a III mohou
členské státy Evropských společenství žádat údaje umožňující
identifikaci těchto zdravotnických prostředků společně s jejich
označením a návody k použití, jestliže jsou tyto zdravotnické
prostředky uváděny do provozu na jejich území; v České republice
uvedené údaje sděluje ministerstvo.
(4) Jestliže výrobce se sídlem nebo místem podnikání
v České republice, který uvádí na trh ve státech Evropských
společenství zdravotnické prostředky podle odstavce 2, nemá
v členském státě zapsané sídlo nebo místo podnikání, jde-li
o právnickou osobu, nebo místo podnikání a trvalý pobyt, jde-li
o fyzickou osobu, pověří na základě písemné smlouvy ve státech
Evropských společenství osobu zodpovědnou za obchodování s těmito
zdravotnickými prostředky, která informuje příslušné orgány
členského státu Evropských společenství, ve kterém má zapsané
sídlo, o adrese tohoto sídla a o kategorii příslušných
zdravotnických prostředků. V České republice informuje osoba
uvedená ve větě první ministerstvo.
(5) Ministerstvo informuje na požádání jiný členský stát
Evropských společenství a Evropskou komisi o podrobnostech
vztahujících se k odstavcům 1 a 2.
------------------------------------------------------------------
19) § 31 odst. 1 až 3 a § 31 odst. 6 zákona č. 123/2000 Sb.
§ 13
Soubor údajů
(1) Údaje
a) o výrobcích, osobách a zdravotnických prostředcích uvedených
v § 12,
b) o vydaných, změněných a zrušených certifikátech, a
c) získané v souladu s postupem upravujícím oznamování a evidenci
nežádoucích příhod20)
se uchovávají v souladu s tímto nařízením v Souboru údajů
z oblasti zdravotnických prostředků shromažďovaných podle hledisek
Evropských společenství, který je přístupný kompetentním úřadům
členských států tak, aby mohly plnit úkoly podle tohoto nařízení.
V České republice je uvedený soubor zřízen a veden v rámci
informačního systému zřízeného podle zákona o zdravotnických
prostředcích;21) jeho uživateli jsou zejména ministerstvo, ústav
v oblasti nežádoucích příhod zdravotnických prostředků, Státní
ústav pro jadernou bezpečnost u zdrojů ionizujícího záření a Ústav
zdravotnických informací a statistiky České republiky.
(2) Údaje uvedené v odstavci 1 se poskytují na formulářích,
jejichž vzory jsou uvedeny v přílohách č. XIX, XX, XXI a XXII
k tomuto nařízení.
------------------------------------------------------------------
20) Vyhláška č. 501/2000 Sb., kterou se stanoví formy, způsoby
ohlašování nežádoucích příhod zdravotnických prostředků,
jejich evidování, šetření a vyhodnocování, dokumentace a její
uchovávání a následné sledování s cílem předcházení vzniku
nežádoucích příhod, zejména jejich opakování (vyhláška
o nežádoucích příhodách zdravotnických prostředků).
21) § 41 zákona č. 123/2000 Sb.
§ 14
Prohlášení o shodě
(1) Při postupu výrobce nebo dovozce podle § 8 musí písemné
prohlášení o shodě obsahovat tyto náležitosti:
a) identifikační údaje o výrobci nebo dovozci, který prohlášení
o shodě vydává, (jméno, příjmení a adresu trvalého pobytu
u fyzické osoby nebo název, popřípadě obchodní firmu a sídlo
u právnické osoby),
b) identifikační údaje o zdravotnickém prostředku [název, typ nebo
číslo modelu, klasifikační třídu podle § 6, u dovážených
zdravotnických prostředků též identifikační údaje o výrobci
podle písmene a)],
c) rozhodné skutečnosti týkající se zdravotnického prostředku
(především určený účel použití a prohlášení, že pro určený účel
použití je zdravotnický prostředek bezpečný, účinný a vhodný
pro použití při poskytování zdravotní péče, popřípadě zda je
sterilní, s měřicí funkcí, zda se jej týkají nebo netýkají jiné
směrnice Evropských společenství, které nejsou převzaty
technickými předpisy),
d) odkazy na technické předpisy,22) způsob posouzení shody, české
technické normy,23) harmonizované normy,8) specifikace použité
při posouzení shody, popřípadě odkazy na ostatní použité
zvláštní právní předpisy,24)
e) název (obchodní firmu), adresu sídla a identifikační číslo
autorizované osoby, jestliže se tato osoba podílela na
posuzování shody,
f) identifikační údaje o osobě, která uchovává technickou
dokumentaci týkající se posuzovaného zdravotnického prostředku,
(jméno, příjmení a adresu trvalého pobytu u fyzické osoby nebo
název, popřípadě obchodní firmu a adresu sídla u právnické
osoby),
g) datum vydání prohlášení o shodě, jména, funkce a podpisy
odpovědných osob výrobce nebo dovozce.
(2) Dojde-li ke změně skutečností, za kterých bylo vydáno
prohlášení o shodě u zdravotnického prostředku, který má být i po
této změně uváděn na trh a do provozu, a pokud tyto změny mohou
ovlivnit vlastnosti zdravotnického prostředku z hlediska
základních požadavků, výrobce nebo dovozce vydá nové prohlášení
o shodě. Jiné změny, které nemění určený účel použití, se uvádějí
v doplňku k prohlášení o shodě.
(3) Jestliže výrobce nebo dovozce postupoval podle § 8,
musí být prohlášení o shodě vypracováno v českém jazyce.
------------------------------------------------------------------
8) § 4a odst. 1 zákona č. 22/1997 Sb., o technických požadavcích
na výrobky a o změně a doplnění některých zákonů, ve znění
zákona č. 71/2000 Sb.
22) § 3 zákona č. 22/1997 Sb., ve znění zákona č. 71/2000 Sb.
23) § 4 odst. 1 zákona č. 22/1997 Sb., ve znění zákona č. 71/2000
Sb.
24) Například zákon č. 18/1997 Sb., o mírovém využívání jaderné
energie a ionizujícího záření (atomový zákon) a o změně
a doplnění některých zákonů, ve znění pozdějších předpisů,
zákon č. 125/1997 Sb., o odpadech, ve znění pozdějších
předpisů, vyhláška č. 142/1997 Sb., o typovém schvalování
obalových souborů pro přepravu, skladování nebo ukládání
radionuklidových zářičů a jaderných materiálů, typovém
schvalování zdrojů ionizujícího záření, typovém schvalování
ochranných pomůcek pro práce se zdroji ionizujícího záření
a dalších zařízení pro práce s nimi (o typovém schvalování),
vyhláška č. 146/1997 Sb., kterou se stanoví činnosti, které
mají bezprostřední vliv na jadernou bezpečnost, a činnosti
zvláště důležité z hlediska radiační ochrany, požadavky na
kvalifikaci a odbornou přípravu, způsob ověřování odborné
způsobilosti a udělování oprávnění vybraným pracovníkům
a způsob provedení schvalované dokumentace pro svolení
k přípravě vybraných pracovníků, vyhláška č. 184/1997 Sb.,
o požadavcích na zajištění radiační ochrany, vyhláška č.
214/1997 Sb., o zabezpečování jakosti při činnostech
souvisejících s využíváním jaderné energie a činnostech
vedoucích k ozáření a o stanovení kritérií pro zařazení
a rozdělení vybraných zařízení do bezpečnostních tříd,
vyhláška č. 219/1997 Sb., o podrobnostech k zajištění
havarijní připravenosti jaderných zařízení a pracovišť se
zdroji ionizujícího záření a o požadavcích na obsah vnitřního
havarijního plánu a havarijního řádu, a vyhláška č. 1/1998
Sb., kterou se stanoví požadavky na jakost, postup při
přípravě, zkoušení, uchovávání a dávkování léčiv (Český
lékopis 1997), ve znění vyhlášky č. 296/1999 Sb.
§ 15
Klinické zkoušky
(1) U zdravotnických prostředků určených pro klinické
zkoušky
a) výrobce nebo dovozce postupuje podle přílohy
1. č. XIV k tomuto nařízení, nebo
2. č. XV k tomuto nařízení, anebo
b) výrobce nebo zplnomocněný zástupce postupuje podle přílohy č.
XV k tomuto nařízení
a oznamuje záměr provést klinické zkoušky příslušnému úřadu
členského státu Evropských společenství, ve kterém mají být tyto
zkoušky prováděny; v České republice tyto osoby oznamují záměr
provést klinické zkoušky ministerstvu a ústavu.
(2) U zdravotnických prostředků třídy III, implantabilních
zdravotnických prostředků a dlouhodobě invazívních zdravotnických
prostředků třídy IIa nebo IIb lze zahájit klinické zkoušky
zdravotnického prostředku po uplynutí 60 dnů po jejich oznámení
podle odstavce 1, pokud jim příslušný orgán členského státu
Evropských společenství, v České republice ministerstvo, neoznámí
během této lhůty nesouhlas s jejich provedením z důvodu ochrany
veřejného zdraví a veřejného zájmu. Tyto zkoušky lze se souhlasem
příslušného orgánu členského státu Evropských společenství zahájit
i před uplynutím 60denní lhůty, pokud příslušná etická komise
vydala souhlas s plánem těchto zkoušek.
(3) Klinické zkoušky musí být prováděny v souladu se
zákonem o zdravotnických prostředcích,10) přílohou č. XVII
k tomuto nařízení a se zvláštními právními předpisy.24)
(4) Ustanovení odstavců 1 a 2 neplatí, jestliže se klinické
zkoušky provádějí u zdravotnických prostředků, u nichž bylo
postupováno podle § 8 nebo § 9, pokud není cílem těchto zkoušek
použití uvedených prostředků pro jiný účel použití, než jim
původně určil výrobce. Příslušná ustanovení přílohy č. XVII
k tomuto nařízení zůstávají nedotčena.
------------------------------------------------------------------
10) § 8 až 16 zákona č. 123/2000 Sb.
24) Například zákon č. 18/1997 Sb., o mírovém využívání jaderné
energie a ionizujícího záření (atomový zákon) a o změně
a doplnění některých zákonů, ve znění pozdějších předpisů,
zákon č. 125/1997 Sb., o odpadech, ve znění pozdějších
předpisů, vyhláška č. 142/1997 Sb., o typovém schvalování
obalových souborů pro přepravu, skladování nebo ukládání
radionuklidových zářičů a jaderných materiálů, typovém
schvalování zdrojů ionizujícího záření, typovém schvalování
ochranných pomůcek pro práce se zdroji ionizujícího záření
a dalších zařízení pro práce s nimi (o typovém schvalování),
vyhláška č. 146/1997 Sb., kterou se stanoví činnosti, které
mají bezprostřední vliv na jadernou bezpečnost, a činnosti
zvláště důležité z hlediska radiační ochrany, požadavky na
kvalifikaci a odbornou přípravu, způsob ověřování odborné
způsobilosti a udělování oprávnění vybraným pracovníkům
a způsob provedení schvalované dokumentace pro svolení
k přípravě vybraných pracovníků, vyhláška č. 184/1997 Sb.,
o požadavcích na zajištění radiační ochrany, vyhláška č.
214/1997 Sb., o zabezpečování jakosti při činnostech
souvisejících s využíváním jaderné energie a činnostech
vedoucích k ozáření a o stanovení kritérií pro zařazení
a rozdělení vybraných zařízení do bezpečnostních tříd,
vyhláška č. 219/1997 Sb., o podrobnostech k zajištění
havarijní připravenosti jaderných zařízení a pracovišť se
zdroji ionizujícího záření a o požadavcích na obsah vnitřního
havarijního plánu a havarijního řádu, a vyhláška č. 1/1998
Sb., kterou se stanoví požadavky na jakost, postup při
přípravě, zkoušení, uchovávání a dávkování léčiv (Český
lékopis 1997), ve znění vyhlášky č. 296/1999 Sb.
§ 16
Autorizované osoby
(1) Podmínky autorizace jsou stanoveny v zákoně25)
a v příloze č. XVIII k tomuto nařízení; o osobách, které vyhoví
požadavkům harmonizovaných norem, se předpokládá, že vyhovují
příslušným kritériím pro autorizaci.
(2) Autorizovaná osoba a
a) výrobce nebo dovozce na základě dohody stanoví termíny pro
dokončení hodnotících a ověřovacích činností uvedených
v přílohách č. II až X k tomuto nařízení,
b) výrobce nebo dovozce na základě dohody stanoví termíny pro
dokončení hodnotících a ověřovacích činností uvedených
v přílohách č. III až XI k tomuto nařízení,
c) výrobce nebo jeho zplnomocněný zástupce na základě dohody
stanoví termíny pro dokončení hodnotících a ověřovacích
činností uvedených v přílohách č. III až XI k tomuto nařízení.
(3) Pokud autorizovaná osoba podle své působnosti zjistí,
že výrobce nesplnil příslušné požadavky tohoto nařízení nebo je
nadále neplní, s výjimkou případů, kdy výrobce zajistil shodu
s těmito požadavky zavedením odpovídajících nápravných opatření,
změní nebo zruší certifikát, který vydala.
(4) Autorizovaná osoba informuje na požádání o vydání,
odmítnutí nebo zrušení certifikátů jiné autorizované osoby, Úřad
pro technickou normalizaci, metrologii a státní zkušebnictví (dále
jen "Úřad") a ministerstvo.
(5) Při informování příslušných úřadů jiných států
a Evropské komise o certifikátech, které autorizovaná osoba
změnila nebo zrušila podle odstavce 3, se postupuje podle
zákona.26)
(6) Úřad poskytne na vyžádání příslušného orgánu jiného
členského státu Evropských společenství informace a dokumenty
k ověření kritérií uvedených v příloze č. XVIII k tomuto nařízení.
------------------------------------------------------------------
25) § 11 zákona č. 22/1997 Sb., ve znění zákona č. 71/2000 Sb.
26) § 7 odst. 5 a 6 zákona č. 22/1997 Sb., ve znění zákona č.
71/2000 Sb.
Ustanovení společná a závěrečná
§ 17
Přechodná ustanovení
Ustanovení § 14 se, s výjimkou zdravotnických prostředků
dovezených ze států, které nejsou členy Evropské unie, nepoužije
ode dne zveřejnění sektorové přílohy "Zdravotnické prostředky"
k Protokolu k Evropské dohodě zakládající přidružení mezi Českou
republikou na jedné straně a Evropskými společenstvími a jejich
členskými státy na straně druhé o posuzování shody a akceptaci
průmyslových výrobků ve Sbírce mezinárodních smluv nebo ode dne
vstupu smlouvy o přistoupení České republiky do Evropské unie
v platnost, bude-li tento den dřívější.
§ 18
Zrušovací ustanovení
Zrušuje se nařízení vlády č. 180/1998 Sb., kterým se
stanoví technické požadavky na prostředky zdravotnické techniky,
ve znění nařízení vlády č. 130/1999 Sb.
§ 19
Účinnost
Toto nařízení nabývá účinnosti dnem vyhlášení, s výjimkou
a) § 3 odst. 6 písm. b), § 4 odst. 2, § 4 odst. 5 písm. b), § 5
odst. 3 písm. b), § 7 odst. 3, § 9, § 11 odst. 3, § 11 odst.
5 písm. b), § 11 odst. 6 písm. b), § 12 odst. 2, § 12 odst. 4,
§ 15 odst. 1 písm. a) bodu 2, § 16 odst. 2 písm. b) a § 16
odst. 5, které nabývají účinnosti dnem zveřejnění sektorové
přílohy "Zdravotnické prostředky" k Protokolu k Evropské dohodě
zakládající přidružení mezi Českou republikou na jedné straně
a Evropskými společenstvími a jejich členskými státy na straně
druhé o posuzování shody a akceptaci průmyslových výrobků ve
Sbírce mezinárodních smluv,
b) příloh č. III, V, VII, IX, XI, XIII a XV k tomuto nařízení,
které nabývají účinnosti podle písmene a); ustanovení týkající
se zplnomocněného zástupce nabývají účinnosti dnem vstupu
smlouvy o přistoupení České republiky do Evropské unie
v platnost, a
c) § 5 odst. 1 písm. b), § 5 odst. 2, § 5 odst. 3 písm. c), § 5
odst. 4, § 7 odst. 4, § 10 odst. 2 písm. b), § 12 odst. 3, § 12
odst. 5, § 15 odst. 1 písm. b) a § 16 odst. 2 písm. c), § 16
odst. 6 tohoto nařízení, které nabývají účinnosti dnem vstupu
smlouvy o přistoupení České republiky do Evropské unie
v platnost.
Předseda vlády:
Ing. Zeman v. r.
Ministr zdravotnictví:
prof. MUDr. Fišer, CSc. v. r.
Příl.I
Základní požadavky
I.
Všeobecné požadavky
1. Zdravotnické prostředky musí být navrženy a vyrobeny tak, aby
při používání za stanovených podmínek a k určenému účelu
použití neohrozily klinický stav, zdraví nebo bezpečnost
pacientů27) nebo bezpečnost a zdraví fyzické nebo právnické
osoby, která poskytuje zdravotní péči (dále jen
"poskytovatel"),28) popřípadě jiných fyzických osob, a to za
předpokladu, že jakákoliv rizika, která mohou s použitím
těchto zdravotnických prostředků souviset, jsou přijatelná
v porovnání s jejich přínosem pro pacienta a odpovídají vysoké
úrovni ochrany zdraví a bezpečnosti.
2. Řešení, která výrobce zvolí při návrhu a konstrukci
zdravotnických prostředků, musí být v souladu se zásadami
bezpečnosti a se současnou úrovní vědy a techniky.
Při výběru nejvhodnějších řešení musí výrobce vycházet
z následujících zásad v uvedeném pořadí:
2.1. vyloučit nebo minimalizovat veškerá rizika (bezpečným
návrhem a konstrukcí) zdravotnických prostředků,
2.2. učinit, kde je to vhodné, odpovídající ochranná opatření
zahrnující v případě potřeby i varování vůči nebezpečím,
která nelze vyloučit,
2.3. informovat uživatele o přetrvávání rizik v důsledku
nedosažení plné dokonalosti uskutečněných ochranných
opatření.
3. Zdravotnické prostředky musí dosahovat účinnosti určené
výrobcem a být navrženy, vyrobeny a zabaleny tak, aby byly
vhodné pro jednu nebo více funkcí uvedených v § 1 odst. 2
v souladu se specifikací jejich výrobce.
4. Při zatížení zdravotnických prostředků, které může nastat za
normálních provozních podmínek, nesmí dojít k nepříznivému
ovlivnění jejich charakteristik a účinnosti ve smyslu bodů 1,
2 a 3 do té míry, aby nedošlo k ohrožení klinických stavů
nebo bezpečnosti pacientů, popřípadě jiných osob, a to po dobu
životnosti zdravotnických prostředků uvedenou výrobcem.
5. Zdravotnické prostředky musí být navrženy, vyrobeny a baleny
tak, aby
5.1. jejich charakteristiky a účinnost pro určený účel použití
nebyly nepříznivě ovlivněny podmínkami dopravy
a skladování při zachování pokynů a informací výrobce,
5.2. umožňovaly snadné používání.
6. Případné vedlejší účinky zdravotnických prostředků musí
představovat pouze přijatelné riziko ve srovnání s jeho
předpokládanými účinky.
II.
Požadavky na návrh a konstrukci zdravotnických prostředků
7. Chemické, fyzikální a biologické vlastnosti zdravotnického
prostředku.
7.1. Zdravotnické prostředky musí být navrženy a vyrobeny tak,
aby byly zaručeny charakteristiky a účinnost uvedené ve
všeobecných požadavcích. Zvláštní pozornost musí být
zaměřena na
7.1.1. výběr materiálů určených pro výrobu a balení
zdravotnických prostředků, zejména z hlediska
toxicity, popřípadě i hořlavosti,
7.1.2. vzájemnou kompatibilitu mezi materiály uvedenými
v bodu 7.1.1. a biologickými tkáněmi, buňkami
a tělesnými tekutinami se zřetelem na určený účel
použití.
7.2. Zdravotnické prostředky musí být navrženy, vyrobeny
a zabaleny tak, aby bylo na nejnižší možnou míru sníženo
riziko vyplývající ze znečištění nežádoucími látkami
a složkami záření a jejich reziduí vůči uživatelům
a osobám podílejícím se na dopravě, skladování
a používání zdravotnických prostředků v souladu s určeným
účelem použití. Zvláštní pozornost musí být věnována
tkáním vystaveným působení uvedených škodlivin, době
trvání a četnosti tohoto působení.
7.3. Zdravotnické prostředky musí být navrženy, vyrobeny
a zabaleny tak, aby mohly být bezpečně použity společně
s látkami a zářením, s nimiž přicházejí do styku
při normálním použití a obvyklých postupech. Jsou-li
zdravotnické prostředky určeny k podávání léčiv, musí být
navrženy a vyrobeny tak, aby při určeném účelu použití
byly s těmito léčivy kompatibilní v mezích ustanovení
a omezení, kterými se tyto výrobky řídí a aby byla
zachována jejich účinnost v souladu s určeným účelem
použití.
7.4. Obsahuje-li zdravotnický prostředek jako integrální
součást látku, která může být při samostatném použití
považována za léčivo a která působí na lidský organismus
prostřednictvím zdravotnického prostředku, musí být
bezpečnost, jakost a účinnost této látky ověřena pro
určený účel použití metodami používanými při zkoušení
léčiv.29)
7.5. Zdravotnické prostředky musí být navrženy a vyrobeny tak,
aby rizika způsobená látkami, popřípadě zářením
unikajícím z nich byla snížena na nejnižší možnou míru.
7.6. Zdravotnické prostředky musí být navrženy a vyrobeny tak,
aby rizika vniknutí nežádoucích látek do nich, s ohledem
na zdravotnický prostředek a povahu prostředí, ve kterém
má být použit, byla snížena na nejnižší možnou míru.
8. Infekce a mikrobiální kontaminace.
8.1. Zdravotnické prostředky a výrobní postupy musí být
navrženy tak, aby se pokud možno vyloučilo nebo snížilo
na nejnižší možnou míru riziko přenosu infekce
zdravotnickým prostředkem na uživatele a jiné fyzické
osoby nebo kontaminace zdravotnického prostředku
uvedenými osobami.
8.2. Tkáně zvířecího původu používané k výrobě zdravotnických
prostředků musí pocházet ze zvířat, nad nimiž byl
vykonáván veterinární dozor v rozsahu odpovídajícím
určenému použití těchto tkání.
8.2.1. Informace o geografickém původu těchto zvířat
uchovávají autorizované osoby.
8.2.2. Zpracování, uchovávání, zkoušení a zacházení
s tkáněmi, buňkami a látkami zvířecího původu musí
být prováděno tak, aby bylo dosaženo optimální
úrovně bezpečnosti, zejména vůči kontaminaci viry
při výrobě zdravotnických prostředků, a to
zavedením validovaných metod určených pro
odstraňování nebo indeaktivaci virů.
8.3. Zdravotnické prostředky dodávané ve sterilním stavu musí
být navrženy, vyrobeny a zabaleny v obalu pro jedno
použití, popřípadě musí být vhodnými postupy zajištěno,
že při uvedení na trh budou sterilní a za stanovených
podmínek skladování a dopravy zůstanou sterilní, dokud
nebude ochranný obal otevřen nebo poškozen.
8.4. Zdravotnické prostředky dodávané ve sterilním stavu musí
být vyrobeny a sterilizovány odpovídajícím schváleným
postupem.30)
8.5. Zdravotnické prostředky, které mají být sterilizovány,
musí být vyrobeny v podmínkách s odpovídající úrovní
kontroly.30)
8.6. Obalové systémy nesterilních zdravotnických prostředků
musí zabezpečovat stanovenou úroveň čistoty
zdravotnického prostředku. Jestliže mají být zdravotnické
prostředky před použitím sterilizovány musí obalové
systémy snižovat riziko mikrobiologické kontaminace na
nejnižší možnou míru. Obalové systémy musí být vhodné pro
použití sterilizační metody stanovené výrobcem.
8.7. Identické nebo podobné zdravotnické prostředky, které
jsou prodávány ve sterilním i v nesterilním stavu musí
být vzájemně rozlišeny obalem nebo označením.
9. Konstrukce a vlastnosti zdravotnického prostředku ve vztahu
k prostředí.
9.1. Je-li zdravotnický prostředek určen k použití ve spojení
s jiným zdravotnickým prostředkem nebo příslušným
vybavením, musí být takto vzniklá souprava včetně
propojovacího systému bezpečná a nesmí narušovat
stanovenou účinnost jednotlivých zdravotnických
prostředků. Jakékoliv omezení použitelnosti musí být
uvedeno v označení zdravotnického prostředku nebo
v návodu k jeho použití.
9.2. Zdravotnické prostředky musí být navrženy a vyrobeny tak,
aby byla odstraněna nebo na nejnižší možnou míru snížena
rizika
9.2.1. poranění vyplývající z fyzikálních charakteristik
zdravotnických prostředků, včetně poměru objemu
a tlaku, rozměrových, popřípadě i ergonomických
charakteristik,
9.2.2. spojená se zdůvodněně předvídatelnými podmínkami
okolního prostředí, zejména magnetickým polem,
vnějšími elektrickými vlivy, elektrostatickými
výboji, tlakem, teplotou nebo změnami v tlaku
a zrychlení,
9.2.3. vzájemného ovlivňování s jinými zdravotnickými
prostředky běžně používanými při určitém
vyšetřování nebo terapii,
9.2.4. vyplývající ze stárnutí použitých materiálů nebo
ztráty přesnosti měřicího, popřípadě kontrolního
mechanismu i ze skutečnosti, že zdravotnické
prostředky nelze udržovat nebo kalibrovat
(implantáty).
9.3. Zdravotnické prostředky musí být navrženy a vyrobeny tak,
aby byla odstraněna nebo na nejnižší možnou míru snížena
rizika požáru nebo výbuchu během normálního použití a za
stavu jedné závady. Zvláštní pozornost je nutno věnovat
zdravotnickým prostředkům, které jsou určeny pro použití
i v prostředí hořlavých látek nebo látek, které
mohou vyvolat hoření.
10. Zdravotnické prostředky s měřicí funkcí.
10.1. Zdravotnické prostředky s měřicí funkcí musí být
navrženy a vyrobeny tak, aby poskytovaly dostatečnou
přesnost a stabilitu v daných mezích přesnosti s ohledem
na jejich určený účel použití; meze přesnosti stanoví
výrobce.
10.2. Stupnice měřidel a displeje musí být řešeny v souladu s
ergonomickými zásadami s ohledem na určený účel použití.
10.3. Výsledky měření provedených zdravotnickými prostředky s
měřicí funkcí musí být vyjádřeny v zákonných jednotkách
v souladu s příslušnou směrnicí ES.31)
11. Ochrana před zářením.
11.1. Obecný požadavek.
11.1.1. Zdravotnické prostředky musí být navrženy a
vyrobeny tak, aby vystavení uživatelů a jiných
fyzických osob účinkům záření bylo s ohledem na
určený účel použití sníženo na nejnižší možnou
míru, aniž by tím bylo omezeno použití
potřebných úrovní záření pro diagnostické a
terapeutické účely.
11.2. Žádoucí záření.
11.2.1. Pokud jsou zdravotnické prostředky určeny k
emitování záření v nebezpečných úrovních, avšak
nezbytných pro specifický zdravotnický účel,
jehož přínos se považuje za odpovídající tomuto
riziku, musí mít uživatel možnost kontrolovat
úroveň těchto emisí. Takové zdravotnické
prostředky musí být navrženy a vyrobeny tak, aby
byla zaručena reprodukovatelnost a tolerance
příslušných proměnných parametrů.
11.2.2. Jestliže jsou zdravotnické prostředky určeny
k emitování potenciálně nebezpečného
viditelného, popřípadě neviditelného záření,
musí být zdravotnické prostředky tam, kde je to
možné, opatřeny displeji, popřípadě doplněné
zvukovými výstrahami, které upozorňují na tyto
emise.
11.3. Nežádoucí záření.
11.3.1. Zdravotnické prostředky musí být navrženy a
vyrobeny tak, aby vystavení uživatelů a jiných
fyzických osob nežádoucímu, neužitečnému nebo
rozptýlenému záření bylo omezeno na nejnižší
možnou míru.
11.4. Návod k použití.
11.4.1. Návod, popřípadě provozní instrukce k použití
zdravotnického prostředku emitujícího záření
musí obsahovat podrobné informace o povaze
emitovaného záření, o prostředcích k ochraně
uživatele a o způsobech zamezení zneužití tohoto
záření a vyloučení rizik plynoucích z instalace
takového zdravotnického prostředku.
11.5. Ionizující záření.32)
11.5.1. Zdravotnické prostředky určené k emitování
ionizujícího záření musí být navrženy a vyrobeny
tak, aby tam, kde to umožňuje určený účel
použití, bylo možné měnit a kontrolovat
množství, geometrii a jakost emitovaného záření.
11.5.2. Zdravotnické prostředky emitující ionizující
záření určené pro radiodiagnostiku musí být
navrženy a vyrobeny tak, aby příslušné jakosti
zobrazení anebo výstupu pro určený medicínský
účel bylo dosaženo při nejmenší možné radiační
zátěži uživatele těchto prostředků.
11.5.3. Zdravotnické prostředky emitující ionizující
záření určené pro radioterapii musí být navrženy
a vyrobeny tak, aby bylo možné spolehlivé
monitorování a řízení dodávané dávky, typu a
energie svazku záření a kde je to potřebné, i
jakosti záření.
12. Požadavky na zdravotnické prostředky připojené ke zdroji
energie nebo vybavené zdrojem energie.
12.1. Zdravotnické prostředky obsahující elektronické
programovatelné systémy musí být navrženy tak, aby byla
zajištěna funkční stálost, spolehlivost a účinnost
těchto systémů v souladu s určeným účelem použití. Při
výskytu závady v tomto systému musí být vhodným způsobem
odstraněna nebo snížena následná rizika na nejnižší
možnou míru.
12.2. Zdravotnické prostředky, u nichž závisí bezpečnost
pacienta na vnitřním zdroji energie, musí být vybaveny
zařízením umožňujícím určit stav zdroje energie.
12.3. Zdravotnické prostředky, u nichž závisí bezpečnost
pacienta na vnějším zdroji energie, musí být vybaveny
varovným systémem k signalizaci výpadku tohoto zdroje.
12.4. Zdravotnické prostředky určené k monitorování jednoho
nebo více klinických údajů pacienta musí být vybaveny
odpovídajícími varovnými systémy, které ohlásí
poskytovateli vznik situace, která by mohla vést k úmrtí
pacienta nebo k závažnému zhoršení jeho zdravotního
stavu.
12.5. Zdravotnické prostředky musí být navrženy a vyrobeny
tak, aby bylo na nejnižší možnou míru sníženo riziko
vzniku elektromagnetických polí, která by mohla narušit
provoz jiných zdravotnických prostředků nebo zařízení v
jejich obvyklém prostředí.33)
12.6. Ochrana před nebezpečím úrazu elektrickým proudem.
Zdravotnické prostředky musí být navrženy a vyrobeny
tak, aby za předpokladu správné instalace a používání
bylo pokud možno vyloučeno nebezpečí náhodného úrazu
elektrickým proudem, a to i za stavu jedné závady.
12.7. Ochrana před nebezpečím vyplývajícím z mechanických a
tepelných vlivů.
12.7.1. Zdravotnické prostředky musí být navrženy a
vyrobeny tak, aby byla zaručena ochrana
uživatele před mechanickým nebezpečím
souvisejícím zejména s pevností, stabilitou a
pohybem některých částí.
12.7.2. Zdravotnické prostředky musí být navrženy a
vyrobeny tak, aby bylo, s přihlédnutím k
současné úrovni vědy a techniky a dostupné
možnosti k omezení vibrací, sníženo na nejnižší
možnou míru nebezpečí vyplývající z vibrací
vyvolaných těmito prostředky, pokud tyto vibrace
nejsou specifickou součástí určeného účelu
použití.
12.7.3. Zdravotnické prostředky musí být navrženy a
vyrobeny tak, aby bylo, s přihlédnutím k
současné úrovni vědy a techniky a dostupné
možnosti k omezení hluku zejména u jeho zdroje,
sníženo na nejnižší možnou míru nebezpečí
vyplývající z jimi emitovaného hluku, pokud
tento hluk není specifickou součástí určené
účinnosti zdravotnických prostředků.
12.7.4. Zdravotnické prostředky musí být navrženy a
vyrobeny tak, aby byla snížena na nejnižší
možnou míru rizika vyplývající z koncových a
připojovacích částí těchto prostředků ke zdrojům
elektrické energie, tlakové kapaliny, vzduchu a
plynu se kterými musí uživatel zacházet.
12.7.5. Zdravotnické prostředky musí být navrženy a
vyrobeny tak, aby jejich přístupné části a
jejich okolí, s výjimkou částí nebo míst
určených k dodávání tepla nebo k dosažení
stanovených teplot, nedosahovaly za normálních
provozních podmínek potenciálně nebezpečných
teplot.
12.8. Ochrana pacienta před nebezpečím vyplývajícím z
dodávaných energií nebo látek.
12.8.1. Zdravotnické prostředky určené k dodávání
energie nebo látek pacientovi musí být navrženy
a vyrobeny tak, aby dodávané množství mohlo být
regulováno s přesností, která zaručuje
bezpečnost uživatele.
12.8.2. Zdravotnické prostředky určené k dodávání
energie nebo látek pacientovi musí být vybaveny
zařízením, které indikuje, popřípadě zabraňuje
dodávání nepřiměřeného množství energie nebo
látek, které by mohlo být nebezpečné.
Zdravotnické prostředky musí být vybaveny
vhodným zařízením, které je schopné v nejvyšší
možné míře zabránit náhodnému uvolnění
nebezpečných množství energie, popřípadě látky z
jejich zdrojů.
12.9. Na zdravotnických prostředcích musí být zřetelně uvedeny
funkce ovládacích prvků a indikátorů.
Jestliže je na zdravotnickém prostředku umístěn návod
potřebný k jeho provozu nebo uvádějící provozní anebo
nastavovací parametry pomocí vizuálního systému, musí
být tyto informace srozumitelné poskytovateli, a pokud
je to vhodné, i pacientovi.
13. Informace poskytované výrobcem nebo dovozcem.
13.1. Zdravotnický prostředek musí být opatřen informacemi
potřebnými k jeho bezpečnému používání a informacemi,
které identifikují jeho výrobce nebo dovozce, a to s
přihlédnutím ke zkušenostem a znalostem potenciálních
uživatelů. Těmito informacemi se rozumějí údaje na
etiketě, popřípadě štítku zdravotnického prostředku a v
návodu k jeho používání; pokud je to proveditelné a
vhodné, musí být tyto informace uvedeny na samotném
zdravotnickém prostředku, na obalu každé jeho části,
popřípadě na obalu, ve kterém se prodává. Není-li
zabalení každé jednotlivé části proveditelné, musí být
informace uvedené v první větě tohoto bodu obsaženy v
návodu k použití dodaném s jedním nebo více
zdravotnickými prostředky.
V balení zdravotnického prostředku musí být přiložen
návod k jeho použití. Tato podmínka nemusí být splněna u
zdravotnického prostředku třídy I nebo IIa, není-li pro
jejich bezpečné používání nezbytně nutné dalších
informací.
13.2. Jestliže je vhodné, aby informace uvedené v bodu 13.1.
byly v podobě symbolů, musí použitý symbol (značka) nebo
identifikační barva vyhovovat normám. V oblastech, pro
které normy neexistují, musí být symboly a barvy popsány
v dokumentaci dodávané se zdravotnickým prostředkem.
13.3. Etiketa nebo štítek zdravotnického prostředku musí
obsahovat, zejména
13.3.1. jméno, příjmení, adresu trvalého pobytu a místa
podnikání, jestliže výrobcem je fyzická osoba
nebo název (obchodní firmu), adresu sídla,
jestliže výrobcem je právnická osoba. U
zdravotnických prostředků dovážených do států
Evropských společenství s předpokladem jejich
distribuce v tomto společenství musí etiketa
nebo štítek nebo vnější obal anebo návod k
použití obsahovat podle okolností adresu
odpovědné osoby podle § 12 odst. 4 nebo
zplnomocněného zástupce anebo dovozce ve státech
Evropských společenství,
13.3.2. podrobné údaje nezbytné pro uživatele k
identifikaci tohoto prostředku a obsahu obalu,
13.3.3. podle potřeby nápis "STERILNÍ",
13.3.4. číslo výrobní dávky (šarže), před kterým je
uvedeno slovo "LOT" nebo výrobní číslo, jestliže
je to možné,
13.3.5. rok a měsíc, do kterého lze tento prostředek
bezpečně použít, jestliže přichází tyto údaje v
úvahu,
13.3.6. údaj, že zdravotnický prostředek je určen pro
jedno použití, jestliže je tento údaj nutný,
13.3.7. nápis "Zakázkový prostředek", jde-li o zakázkový
zdravotnický prostředek,
13.3.8. nápis "Pouze pro klinické zkoušky", jestliže je
zdravotnický prostředek určen pro tento účel,
13.3.9. zvláštní podmínky jeho skladování, popřípadě
zacházení s ním,
13.3.10. zvláštní provozní pokyny,
13.3.11. výstrahy, popřípadě i jiná nutná opatření,
13.3.12. rok výroby, jde-li o aktivní zdravotnický
prostředek, pokud se u něho neuvádí obsah bodu
13.3.5.; tento údaj může být součástí čísla
výrobní dávky (šarže) nebo sériového čísla,
pokud je z těchto údajů snadno odvoditelný,
13.3.13. postup při sterilizaci tohoto prostředku,
jestliže přichází v úvahu.
13.4. Jestliže lze důvodně předpokládat, že určený účel
použití zdravotnického prostředku nemusí být uživateli
zřejmý, výrobce nebo dovozce jej uvede v označení
zdravotnického prostředku a v návodu k jeho použití.
13.5. Pokud je účelné a proveditelné, musí být zdravotnický
prostředek a jeho odnímatelné součásti označeny, zejména
údaji o výrobní dávce nebo šarži, aby při určeném účelu
použití bylo možné zjistit rizika představovaná
zdravotnickými prostředky a jejich součástmi.
13.6. Návod k použití, není-li to povahou zdravotnického
prostředku vyloučeno, musí obsahovat:
13.6.1. podrobné údaje uvedené v bodu 13.3., s výjimkou
bodu 13.3.4. a bodu 13.3.5. této přílohy,
13.6.2. údaje o účinnosti zdravotnického prostředku
podle bodu 3. této přílohy, jakož i vedlejší
nežádoucí účinky,
13.6.3. podrobné údaje o charakteristikách
zdravotnického prostředku, aby bylo možné určit
správné zdravotnické prostředky nebo vybavení,
jejichž použitím vznikne bezpečný systém nebo
souprava, a to jestliže jde o zdravotnické
prostředky, které podle určeného účelu použití
musí být instalovány nebo spojeny s dalšími
zdravotnickými prostředky nebo vybavením,
13.6.4. informace potřebné pro ověření, zda zdravotnický
prostředek je řádně instalován a může být
správně a bezpečně provozován, včetně potřebných
údajů o povaze a četnosti údržby a kalibraci,
které jsou nezbytné k řádné a bezpečné funkci,
13.6.5. informace o možnostech odvrácení nebezpečí
souvisejících s implantací zdravotnického
prostředku, jestliže je to potřebné,
13.6.6. informace týkající se nebezpečí vzájemné
ovlivňovatelnosti mezi zdravotnickými prostředky
přítomnými během specifických vyšetření nebo
terapie,
13.6.7. pokyny nezbytné pro případ poškození sterilního
obalu, popřípadě údaje o vhodných postupech při
opětovné sterilizaci,
13.6.8. informace o vhodných postupech, které umožňují
opakované použití zdravotnického prostředku, a
to včetně čištění, dezinfekce, balení, popřípadě
vhodných postupech opětovné sterilizace
zdravotnického prostředku, a doporučovaném počtu
opakovaných použití, jestliže je zdravotnický
prostředek určen k opakovanému použití.
Jestliže je zdravotnický prostředek dodán s tím,
že má být před použitím sterilizován, musí být
návod na čištění a sterilizaci takový, aby při
jeho dodržení zdravotnický prostředek trvale
vyhovoval požadavkům uvedeným v části I. této
přílohy (Všeobecné požadavky),
13.6.9. údaje o zacházení se zdravotnickým prostředkem
před jeho vlastním použitím, zejména o
sterilizaci, popřípadě o konečné sestavě
zdravotnických prostředků,
13.6.10. údaje o povaze, typu, intenzitě a rozložení
emitujícího záření u zdravotnických prostředků
emitujících záření pro zdravotnické účely,
13.6.11. podrobné údaje, které umožní poskytovateli
poučit pacienta o kontraindikacích a nutných
předběžných opatřeních, která je nutno provést
v případě změn účinnosti zdravotnického
prostředku,
13.6.12. opatrnost, kterou je nutno za předvídatelných
podmínek prostředí dodržovat, a to zejména s
ohledem na účinky magnetických polí, vnějších
elektrických vlivů, elektrostatických výbojů,
tlaků nebo změn tlaku, zrychlení, zdrojů
tepelného vzplanutí,
13.6.13. přiměřené informace o léčivu, výrobcích,
popřípadě látkách, které se prostřednictvím
zdravotnického prostředku aplikují, včetně
omezení výběru látek, které mají být podávány,
13.6.14. informace týkající se opatrnosti, opatření
nutná pro bezpečné zneškodňování zdravotnických
prostředků, zejména pro případy neobvyklých
rizik souvisejících s touto činností,
13.6.15. informace o léčivech, která jsou integrální
součástí zdravotnického prostředku podle bodu
7.4. této přílohy,
13.6.16. stupeň přesnosti vyžadovaný u zdravotnických
prostředků s měřicí funkcí.
14. Jestliže se požaduje, aby shoda se základními požadavky
vycházela z klinických údajů obdobně jako v bodu 6., musí být
tyto údaje stanoveny v souladu se zákonem o zdravotnických
prostředcích10) a přílohou č. XVII k tomuto nařízení.
------------------------------------------------------------------
10) § 8 až 16 zákona č. 123/2000 Sb.
27) § 3 písm. e) zákona č. 123/2000 Sb.
28) § 3 písm. d) zákona č. 123/2000 Sb.
29) Vyhláška č. 1/1998 Sb., ve znění vyhlášky č. 296/1999 Sb.
30) Bod 2.6.1 a násl. vyhlášky č. 1/1998 Sb., ve znění vyhlášky č.
296/1999 Sb.
31) Směrnice Rady 80/181/EHS, ve znění směrnice Rady 89/617/EHS.
32) Zákon č. 18/1997 Sb.
33) § 32 odst. 1 zákona č. 123/2000 Sb.
Příl.II
Posouzení systému jakosti autorizovanou osobou
(Systém úplného zabezpečení jakosti)
1. Posouzení systému jakosti autorizovanou osobou je postup,
kterým výrobce nebo dovozce zaručuje a prohlašuje, že
příslušné zdravotnické prostředky, pro jejichž návrh, výrobu a
výstupní kontrolu výrobce zajistil uplatnění systému jakosti,
vyhovují ustanovením, která se na ně vztahují z tohoto
nařízení.
2. Výrobce nebo dovozce
2.1. postupuje v označování zdravotnických prostředků v
souladu s § 4 odst. 1,
2.2. vypracuje písemné prohlášení o shodě podle § 14, toto
prohlášení musí zahrnovat příslušný počet vyrobených
zdravotnických prostředků a musí být uchováváno u výrobce
nebo dovozce.
2a. Výrobce podléhá auditu podle bodů 3.3., 4. a 5. této přílohy.
3. Systém jakosti.
3.1. Výrobce nebo dovozce
3.1.1. předkládá písemnou žádost autorizované osobě o
posouzení (vyhodnocení a schválení) systému
jakosti pro návrh, výrobu a výstupní kontrolu
konkrétních zdravotnických prostředků; žádost musí
obsahovat
3.1.1.1. jméno, příjmení a adresu trvalého pobytu
výrobce, jestliže jde o fyzickou osobu,
název (obchodní firmu) a adresu sídla,
je-li výrobcem právnická osoba; v obou
případech včetně adres výrobních míst,
pro která platí systém jakosti,
3.1.1.2. odpovídající informace o zdravotnickém
prostředku nebo o kategorii
zdravotnických prostředků, pro které
platí postup uvedený v bodu 1,
3.1.1.3. písemné prohlášení, že u jiné
autorizované osoby nebyla podána žádost
pro systém jakosti vztahující se ke
stejnému zdravotnickému prostředku,
3.1.1.4. dokumentaci systému jakosti,
3.1.1.5. záruku výrobce plnit závazky vyplývající
ze schváleného systému jakosti,
3.1.1.6. záruku výrobce udržovat systém jakosti v
přiměřeném a účinném stavu,
3.1.1.7. záruku výrobce, že zavede a bude
aktualizovat systematický postup
získávání a vyhodnocování informací
a zkušeností získaných v době po
vyskladnění od výrobce a v návaznosti na
uvedenou činnost provádět odpovídající
nápravná opatření, zejména oznamovat
vznik nežádoucích příhod,14) jakmile se
o nich dozví.
3.2. Uplatňovaný systém jakosti musí zajistit jakost výroby
zdravotnických prostředků tak, aby vyrobené zdravotnické
prostředky odpovídaly ustanovením, která se na ně
vztahují z tohoto nařízení, a to v každém stadiu od
jejich návrhu až po výstupní kontrolu.
Prvky, požadavky a opatření učiněná výrobcem pro jím
uplatňovaný systém jakosti musí být systematicky a řádně
dokumentovány formou písemně vypracovaných programů a
postupů, a to programy jakosti, plány jakosti, příručkami
jakosti a záznamy o jakosti.
Dokumentace systému jakosti musí obsahovat, zejména popis
3.2.1. cílů jakosti výrobce,
3.2.2. organizace výrobce, zejména
3.2.2.1. organizačních struktur, zodpovědnosti
vedoucích zaměstnanců a jejich pravomocí
ve vztahu k jakosti návrhu a zhotovení
zdravotnického prostředku,
3.2.2.2. metod sledování účinnosti systému
jakosti, především jeho schopnosti
dosáhnout požadované jakosti návrhu
zdravotnického prostředku, včetně
kontroly těch zdravotnických prostředků,
které požadované jakosti nedosáhnou
(nebylo u nich dosaženo shody),
3.2.3. postupů pro sledování a ověřování návrhu
zdravotnických prostředků, především
3.2.3.1. všeobecný popis zdravotnického
prostředku, včetně plánovaných variant,
3.2.3.2. specifikace návrhu, včetně norem, které
budou použity, výsledků analýzy rizik a
popis řešení přijatých ke splnění
základních požadavků platných pro
zdravotnické prostředky, jestliže normy
nejsou použity v plném rozsahu,
3.2.3.3. techniky řízení a ověřování návrhů,
postupů a systematických opatření,
používaných při navrhování zdravotnického
prostředku,
3.2.3.4. důkazu, že zdravotnický prostředek, který
je určen k použití ve spojení s jinými
zdravotnickými prostředky, vyhovuje
základním požadavkům a má charakteristiky
specifikované výrobcem, a to i po
připojení k těmto jiným zdravotnickým
prostředkům,
3.2.3.5. prohlášení, zda prostředek obsahuje či
neobsahuje jako svou integrální část
látku, která může být při samostatném
použití považována za léčivo, spolu s
údaji o příslušných provedených
zkouškách,
3.2.3.6. návrh označení a podle potřeby i návod k
použití,
3.2.3.7. klinické údaje získané podle zákona o
zdravotnických prostředcích10) a přílohy
č. XVII k tomuto nařízení,
3.2.4. techniky kontrol a zabezpečení jakosti ve stadiu
výroby zdravotnického prostředku, zejména
3.2.4.1. postupy a procedury, které budou použity
pro sterilizaci a prodej včetně
příslušných dokumentů,
3.2.4.2. postupy k identifikaci zdravotnického
prostředku vypracované a aktualizované ve
všech stadiích výroby na základě výkresů,
specifikací a dalších odpovídajících
dokumentů,
3.2.5. příslušné testy a zkoušky, které budou vykonány
před výrobou, během výroby a po výrobě
zdravotnických prostředků, jejich četnost a
použitá zkušební zařízení; zpětně musí být možné
přiměřeným způsobem zjistit správnost kalibrace
zkušebních zařízení.
3.3. Autorizovaná osoba provádí audity systému jakosti za
účelem zjištění, zda systém jakosti vyhovuje požadavkům
uvedeným v bodu 3.2. této přílohy. Shoda s těmito
požadavky se předpokládá u systémů jakosti, které
používají odpovídající normy. V týmu pověřeném hodnocením
systému jakosti musí být alespoň jeden člen, který má
zkušenosti s hodnocením příslušných technologií.
Hodnotitelský postup zahrnuje prohlídku provozních
prostor výrobce a v odůvodněných případech i kontrolu
výrobních postupů v provozních prostorech dodavatelů
výrobce, popřípadě jeho dalších smluvních stran.
Autorizovaná osoba oznámí výrobci, po provedeném auditu
systému jakosti, rozhodnutí, které musí obsahovat závěry
kontroly a odůvodněné zhodnocení.
3.4. Výrobce nebo dovozce informuje autorizovanou osobu, která
schválila systém jakosti, o záměru, který podstatně mění
systém jakosti nebo jím pokrytý okruh zdravotnických
prostředků.
Autorizovaná osoba zhodnotí navrhované změny, ověří, zda
takto změněný systém jakosti ještě vyhovuje požadavkům
uvedeným v bodu 3.2. této přílohy a oznámí své rozhodnutí
výrobci nebo dovozci; toto rozhodnutí musí obsahovat
závěry kontroly a odůvodněné zhodnocení.
4. Přezkoumání návrhu zdravotnického prostředku.
4.1. Výrobce nebo dovozce požádá, vedle svých úkolů podle bodu
3. této přílohy, autorizovanou osobu o přezkoumání
dokumentace k návrhu zdravotnického prostředku, který má
výrobce v úmyslu vyrábět a který patří do kategorie
zdravotnických prostředků podle bodu 3.1. této přílohy.
4.2. Žádost musí popisovat návrh a výrobu; v žádosti výrobce
uvádí i údaje o účinnosti zdravotnického prostředku,
který má v úmyslu vyrábět. K žádosti připojuje dokumenty,
které umožní posoudit, zda zdravotnický prostředek
splňuje požadavky podle bodu 3.2.3. této přílohy.
4.3. Autorizovaná osoba
4.3.1. přezkoumá žádost, a jestliže zdravotnický
prostředek vyhovuje ustanovením tohoto nařízení
vydá žadateli certifikát o přezkoumání návrhu
zdravotnického prostředku (dále jen "certifikát o
přezkoumání návrhu").
Certifikát o přezkoumání návrhu musí obsahovat
závěry přezkoumání, podmínky platnosti, údaje
potřebné k identifikaci schváleného návrhu
zdravotnického prostředku a jeho výrobce,
popřípadě popis určeného účelu použití,
4.3.2. vyžádá, podle svého uvážení, doplnění žádosti
dalšími zkouškami nebo důkazy, které jí umožní
posoudit shodu zdravotnického prostředku s
požadavky tohoto nařízení,
4.3.3. projedná před vydáním rozhodnutí postup s ústavem,
jde-li o zdravotnický prostředek, který obsahuje
jako integrální součást léčivo. Autorizovaná osoba
při svém rozhodování přihlédne k výsledkům tohoto
projednání a své konečné rozhodnutí oznámí ústavu.
4.4. Autorizovaná osoba, která vydala certifikát o přezkoumání
návrhu, dodatečně schvaluje změny schváleného návrhu
zdravotnického prostředku, které by mohly ovlivnit shodu
se základními požadavky nebo podmínky předepsané pro
použití zdravotnického prostředku.
Žadatel informuje autorizovanou osobu, která vydala
certifikát o přezkoumání návrhu, o změnách schváleného
návrhu zdravotnického prostředku, které by mohly ovlivnit
shodu se základními požadavky tohoto nařízení.
Uvedené doplňkové schválení návrhu vydává autorizovaná
osoba jako dodatek k certifikátu o přezkoumání návrhu.
5. Dozor.
5.1. Cílem dozoru je zajistit, aby výrobce náležitě plnil
závazky vyplývající ze schváleného systému jakosti.
5.2. Za účelem uvedeným v bodu 5.1. této přílohy výrobce
zmocňuje autorizovanou osobu k provádění nezbytných
kontrol a poskytuje jí příslušné informace, zejména
5.2.1. dokumentaci systému jakosti,
5.2.2. údaje vyhrazené systémem jakosti pro oblast návrhu
zdravotnického prostředku, především výsledky
analýz, propočtů a zkoušek,
5.2.3. údaje vyhrazené systémem jakosti pro oblast výroby
zdravotnického prostředku, především zprávy o
kontrolách, zkouškách, kalibraci a o kvalifikaci
příslušných zaměstnanců.
5.3. Autorizovaná osoba
5.3.1. provádí periodicky příslušné kontroly a hodnocení
tak, aby se ujistila, že výrobce používá schválený
systém jakosti a
5.3.2. poskytuje výrobci hodnotící zprávu,
5.3.3. provádí, podle svého uvážení, u výrobce i předem
neohlášené kontroly, při nichž je oprávněna v
případě potřeby provést nebo si vyžádat provedení
zkoušky za účelem kontroly, zda systém jakosti je
řádně účinný.
5.4. Autorizovaná osoba poskytuje výrobci zprávu o provedené
kontrole, popřípadě i o výsledku zkoušky, jestliže byla
provedena.
6. Administrativní opatření.
6.1. Výrobce uchovává nebo dovozce zpřístupní po dobu nejméně
5 let po vyrobení posledního zdravotnického prostředku
pro potřebu příslušných orgánů státní správy
6.1.1. písemné prohlášení o shodě,
6.1.2. dokumentaci systému jakosti,
6.1.3. změny podle bodu 3.4. této přílohy,
6.1.4. dokumentaci podle bodu 4.2. této přílohy.
6.2. V případě, že výrobce nemá sídlo v České republice
uchovává přístup k dokumentaci zdravotnického prostředku,
který podléhá postupu podle bodu 4., dovozce nebo osoba,
která uvádí tento prostředek na trh v České republice.
7. Použití pro zdravotnické prostředky tříd IIa a IIb.
V souladu s § 8 odst. 2 a 3 lze tuto přílohu, s výjimkou bodu
4, použít pro zdravotnické prostředky tříd IIa a IIb.
------------------------------------------------------------------
10) § 8 až 16 zákona č. 123/2000 Sb.
14) § 14 zákona č. 22/1997 Sb., ve znění zákona č. 71/2000 Sb.
Příl.III
ES prohlášení o shodě
(Systém úplného zabezpečení jakosti)
1. Jestliže výrobce zvolí postup posuzování shody u
zdravotnických prostředků podle § 9 odst. 1 písm. a) nebo
odst. 3 písm. a), zajišťuje pro jejich návrh, výrobu včetně
výstupní kontroly uplatňování systému jakosti podle bodu 3.;
při uvedených činnostech podléhá auditu podle bodu 3.3. a 4. a
dozoru podle bodu 5.
2. Výrobce
2.1. označuje zdravotnické prostředky v souladu s § 4 odst. 2,
2.2. vypracuje písemné prohlášení o shodě; toto prohlášení je
postup, kterým výrobce plnící požadavky vyplývající z
činnosti v bodu 1., zaručuje a prohlašuje, že příslušné
zdravotnické prostředky vyhovují ustanovením, která se na
ně vztahují z tohoto nařízení.
3. Systém jakosti.
3.1. Výrobce
3.1.1. předkládá písemnou žádost autorizované osobě o
posouzení (vyhodnocení a schválení) jeho systému
jakosti; žádost musí obsahovat
3.1.1.1. jméno, příjmení a adresu trvalého pobytu
výrobce, jestliže jde o fyzickou osobu,
název (obchodní firmu) a adresu sídla,
je-li výrobcem právnická osoba; v obou
případech včetně adres výrobních míst,
pro která platí systém jakosti,
3.1.1.2. odpovídající informace o zdravotnickém
prostředku nebo o kategorii
zdravotnických prostředků, pro které
postup platí,
3.1.1.3. písemné prohlášení, že u jiné
autorizované osoby nebyla podána žádost
pro systém jakosti vztahující se ke
stejnému zdravotnickému prostředku,
3.1.1.4. dokumentaci systému jakosti,
3.1.1.5. záruku výrobce plnit závazky vyplývající
ze schváleného systému jakosti,
3.1.1.6. záruku výrobce udržovat systém jakosti v
přiměřeném a činném stavu,
3.1.1.7. záruku výrobce, že zavede a bude
aktualizovat systematický postup
vyhodnocování zkušeností získaných o
zdravotnických prostředcích od uživatelů
a v návaznosti na tuto činnost provádět
odpovídající nápravná opatření, zejména
oznamovat vznik nežádoucích příhod33)
ihned jakmile se o nich dozví.
3.2. Požadavky na dokumentaci systému jakosti musí obsahovat
údaje uvedené v bodu
3.2. přílohy č. II k tomuto nařízení.
3.3. Pro postup autorizované osoby týkající se auditů
jakosti se použije ustanovení bodu 3.3. přílohy č.
II k tomuto nařízení.
3.4. Výrobce informuje autorizovanou osobu, která
schválila systém jakosti o záměru, který podstatně
mění systém jakosti nebo jím pokrytý okruh
zdravotnických prostředků.
Autorizovaná osoba zhodnotí navrhované změny, ověří,
zda takto změněný systém jakosti ještě vyhovuje
požadavkům uvedeným v bodu 3.2. této přílohy a
oznámí své rozhodnutí výrobci; toto rozhodnutí musí
obsahovat závěry kontroly a odůvodněné zhodnocení.
4. Přezkoumání návrhu zdravotnického prostředku.
4.1. a 4.2. Pro postup výrobce při přezkoumání návrhu
zdravotnického prostředku se použije ustanovení bodu 4.1.
a 4.2. přílohy č. II k tomuto nařízení.
4.3. Autorizovaná osoba
4.3.1. přezkoumá žádost, a jestliže zdravotnický
prostředek vyhovuje ustanovením tohoto nařízení
vydá žadateli ES certifikát o přezkoumání návrhu
zdravotnického prostředku (dále jen "ES certifikát
o přezkoumání návrhu").
ES certifikát o přezkoumání návrhu musí obsahovat
závěry přezkoumání, podmínky platnosti, údaje
potřebné k identifikaci schváleného návrhu
zdravotnického prostředku a jeho výrobce,
popřípadě popis určeného účelu použití,
4.3.2. vyžádá, podle svého uvážení, doplnění žádosti
dalšími zkouškami nebo důkazy, které jí umožní
posoudit shodu zdravotnického prostředku s
požadavky tohoto nařízení,
4.3.3. projedná před vydáním rozhodnutí postup s
příslušným orgánem členského státu Evropských
společenství, v České republice s ústavem, jde-li
o zdravotnický prostředek, který obsahuje jako
integrální součást léčivo. Autorizovaná osoba při
svém rozhodování přihlédne k výsledkům tohoto
projednání a své konečné rozhodnutí sdělí
příslušnému orgánu členského státu Evropských
společenství, v České republice ústavu.
4.4. Autorizovaná osoba, která vydala ES certifikát o
přezkoumání návrhu, dodatečně schvaluje změny schváleného
návrhu zdravotnického prostředku, které by mohly ovlivnit
shodu se základními požadavky nebo podmínky předepsané
pro použití zdravotnického prostředku.
Žadatel informuje autorizovanou osobu, která vydala ES
certifikát o přezkoumání návrhu, o změnách schváleného
návrhu zdravotnického prostředku, které by mohly ovlivnit
shodu se základními požadavky tohoto nařízení.
Uvedené doplňkové schválení návrhu vydává autorizovaná
osoba jako dodatek k ES certifikátu o přezkoumání návrhu
zdravotnického prostředku.
5. Dozor.
5.1. Pro dozor se použije ustanovení bodu 5. přílohy č. II k
tomuto nařízení.
6. Administrativní opatření.
6.1. Pro postup výrobce při uchování dokumentace se použije
ustanovení bodu 6.1. přílohy č. II k tomuto nařízení.
6.2. Není-li ve státech Evropských společenství ustanoven
výrobce ani jeho zplnomocněný zástupce, udržuje přístup
k technické dokumentaci týkající se zdravotnických
prostředků podléhajících postupu podle bodu 4. osoba,
která uvádí zdravotnické prostředky na trh ve státech
Evropských společenství nebo dovozce podle přílohy č.
I bodu 13.3.1. k tomuto nařízení.
7. Použití pro zdravotnické prostředky tříd IIa a IIb.
V souladu s § 9 odst. 2 a 3 lze tuto přílohu, s výjimkou bodu
4., použít pro zdravotnické prostředky tříd IIa a IIb.
------------------------------------------------------------------
33) § 32 odst. 1 zákona č. 123/2000 Sb.
Příl.IV
Přezkoušení typu zdravotnického
prostředku autorizovanou osobou
1. Přezkoušení typu zdravotnického prostředku autorizovanou osobu
je postup, při kterém autorizovaná osoba zjišťuje, zda
reprezentativní vzorek posuzované výroby zdravotnických
prostředků (dále jen "typ") splňuje příslušná ustanovení
tohoto nařízení, která se na něj vztahují a v kladném případě
vydá certifikát o přezkoušení typu; ve spojitosti s tím
výrobce nebo dovozce zaručuje a prohlašuje, že zdravotnické
prostředky dodávané na trh odpovídají certifikovanému typu.
2. Výrobce nebo dovozce požádá autorizovanou osobu o přezkoušení
typu zdravotnického prostředku; žádost obsahuje
2.1. jméno, příjmení a adresu trvalého pobytu výrobce,
jestliže jde o fyzickou osobu, název (obchodní firmu) a
adresu sídla, je-li výrobcem právnická osoba,
2.2. dokumentaci podle bodu 3 této přílohy, která je potřebná
k posouzení shody typu s požadavky tohoto nařízení.
Žadatel předá typ autorizované osobě, která si podle
svého uvážení vyžádá další vzorky,
2.3. písemné prohlášení, že stejná žádost nebyla podána jiné
autorizované osobě.
3. Dokumentace musí umožnit porozumění návrhu, výrobě a činnosti
zdravotnického prostředku a musí obsahovat zejména
3.1. všeobecný popis typu, včetně zamýšlených variant,
3.2. konstrukční výkresy, připravované výrobní technologie,
zvláště jde-li o sterilizaci a schémata součástí,
podsestav a obvodů,
3.3. popisy a vysvětlivky nezbytné k porozumění konstrukčním
výkresům, schématům a činnosti zdravotnického prostředku,
3.4. seznam norem, jejichž druhy jsou uvedeny v § 3 odst. 2 a
3, které byly úplně nebo částečně použity a popisy řešení
pro dodržení základních požadavků, pokud uvedené normy
nebyly plně použity,
3.5. výsledky konstrukčních výpočtů, analýzy rizik, výzkumu a
technických zkoušek,
3.6. údaj, zda zdravotnický prostředek obsahuje jako
integrální část léčivo spolu s údaji o zkouškách
provedených v této souvislosti,
3.7. klinické údaje podle přílohy č. XVII k tomuto nařízení,
3.8. návrh označení, a kde je to vhodné, návod k použití
zdravotnického prostředku.
4. Autorizovaná osoba
4.1. přezkoumá a zhodnotí dokumentaci a ověří, zda byl typ
vyroben v souladu s touto dokumentací. O požadavcích,
které jsou navrhovány v souladu s příslušnými normami
uvedenými v § 3 odst. 2 a 3 a o skutečnostech, které
nejsou navrhovány podle těchto norem, pořídí záznam,
4.2. provede nebo nechá provést příslušné kontroly a zkoušky
nezbytné k ověření, zda řešení přijatá výrobcem splňují
základní požadavky, a to v případě nepoužití norem
uvedených v § 3 odst. 2 a 3. Jestliže pro určený účel
použití má být zdravotnický prostředek spojen s jiným
zdravotnickým prostředkem, popřípadě jinými
zdravotnickými prostředky, musí být prokázáno, že systém
nebo souprava jako celek vyhovuje základním požadavkům,
jestliže je připojen k takovému prostředku nebo
prostředkům, pokud má (mají) charakteristiky
specifikované výrobcem,
4.3. provede nebo nechá provést příslušné kontroly nebo
zkoušky nezbytné k ověření, zda výrobce skutečně použil
odpovídající normy, které zvolil,
4.4. dohodne se žadatelem místo, kde budou nezbytné kontroly a
zkoušky prováděny.
5. Autorizovaná osoba
5.1. vydá žadateli certifikát o přezkoušení typu, jestliže typ
splňuje ustanovení tohoto nařízení.
Certifikát musí obsahovat
5.1.1. jméno, příjmení a adresu trvalého pobytu výrobce,
jestliže jde o fyzickou osobu; název (obchodní
firmu) a adresu sídla výrobce, jestliže jde o
právnickou osobu,
5.1.2. závěry, kontroly, podmínky platnosti a údaje
potřebné k identifikaci schváleného typu.
Příslušné části dokumentace musí být připojeny k
certifikátu o přezkoušení typu,
5.2. uchovává kopie certifikátu a příslušné části dokumentace
připojené k certifikátu o přezkoušení typu,
5.3. projedná, v případě zdravotnických prostředků, které
obsahují jako integrální součást léčivo, před vydáním
rozhodnutí postup s ústavem. Autorizovaná osoba při svém
rozhodování přihlédne k výsledkům tohoto projednání,
konečné rozhodnutí postoupí ústavu.
6. Výrobce nebo dovozce informuje autorizovanou osobu, která
vydala certifikát o přezkoušení typu, o podstatné změně, která
má být provedena na schváleném zdravotnickém prostředku.
6.1. Autorizovaná osoba, která vydala certifikát o přezkoušení
typu vydá dodatečně souhlas s návrhem změny schváleného
zdravotnického prostředku, a to pouze v případě, jestliže
tyto změny mohou ovlivnit shodu se základními požadavky
nebo s podmínkami stanovenými pro použití zdravotnického
prostředku. Uvedený dodatečný souhlas musí mít formu
dodatku k původnímu certifikátu o přezkoušení typu.
7. Administrativní opatření.
7.1. Autorizované osoby mohou obdržet kopie certifikátů o
přezkoušení typu, popřípadě jejich dodatků. Přílohy
certifikátů musí být dostupné jiným autorizovaným osobám
na základě odůvodněné žádosti a po předchozím informování
výrobce nebo dovozce.
7.2. Výrobce uchovává s technickou dokumentací zdravotnického
prostředku kopie certifikátů o přezkoušení typu a jejich
dodatky po dobu nejméně 5 let po vyrobení posledního
zdravotnického prostředku.
7.3. Jestliže výrobce nemá v České republice sídlo, udržuje
přístup k technické dokumentaci zdravotnického prostředku
dovozce, popřípadě osoba odpovědná za uvedení
zdravotnického prostředku na trh v České republice.
Příl.V
ES přezkoušení typu
1. ES přezkoušení typu zdravotnického prostředku je postup,
kterým autorizovaná osoba zjišťuje a certifikuje, že
reprezentativní vzorek posuzované výroby zdravotnických
prostředků (dále jen "typ") splňuje příslušná ustanovení
tohoto nařízení, která se na něj vztahují.
2. Výrobce, popřípadě zplnomocněný zástupce požádá autorizovanou
osobu o přezkoušení typu zdravotnického prostředku; žádost
obsahuje:
2.1. jméno, příjmení a adresu trvalého pobytu výrobce,
jestliže jde o fyzickou osobu, název (obchodní firmu) a
adresu sídla, je-li výrobcem právnická osoba; jméno,
příjmení a trvalý pobyt zplnomocněného zástupce, jestliže
podává žádost jako fyzická osoba, název (obchodní firmu)
a adresu sídla, podává-li žádost jako právnická osoba,
2.2. dokumentaci uvedenou v příloze č. IV bodu 2.2. k tomuto
nařízení a
2.3. písemné prohlášení podle přílohy č. IV bodu 2.3. k tomuto
nařízení.
3. Dokumentace musí splňovat požadavky uvedené v příloze č. IV
bodu 3. k tomuto nařízení.
4. Autorizovaná osoba postupuje podle přílohy č. IV bodu 4 k
tomuto nařízení.
5. Autorizovaná osoba
5.1. vydá žadateli ES certifikát o přezkoušení typu, jestliže
typ splňuje ustanovení tohoto nařízení. ES certifikát
musí obsahovat náležitosti uvedené v příloze č. IV bodech
5.1.1. a 5.1.2. k tomuto nařízení,
5.2. uchovává kopie ES certifikátu a příslušné části
dokumentace připojené k ES certifikátu o přezkoušení typu
a
5.3. postupuje, v případě zdravotnických prostředků
obsahujících jako integrální součást léčivo podle přílohy
č. IV bodu 5.3. k tomuto nařízení.
6. Výrobce, popřípadě zplnomocněný zástupce informuje
autorizovanou osobu, která vydala ES certifikát o přezkoušení
typu o podstatné změně, kterou zamýšlí provést na schváleném
zdravotnickém prostředku.
6.1. Autorizovaná osoba, která vydala ES certifikát o
přezkoušení typu, vydá dodatečně souhlas s návrhem změny
schváleného zdravotnického prostředku, a to pouze v
případě, že tyto změny mohou ovlivnit shodu se základními
požadavky nebo s podmínkami stanovenými pro použití
zdravotnického prostředku. Uvedený dodatečný souhlas musí
mít formu dodatku k původnímu ES certifikátu o
přezkoušení typu.
7. Administrativní opatření.
7.1. Autorizované osoby mohou obdržet kopie ES certifikátů o
přezkoušení typu, popřípadě jejich dodatků. Přílohy ES
certifikátů musí být dostupné jiným autorizovaným osobám
na základě odůvodněné žádosti po předchozím informování
výrobce.
7.2. Výrobce nebo jeho zplnomocněný zástupce uchovává s
technickou dokumentací kopie ES certifikátů o přezkoušení
typu a jejich dodatky po dobu nejméně 5 let po vyrobení
posledního zdravotnického prostředku.
7.3. Jestliže výrobce nemá ve státech Evropských společenství
ani v České republice zapsané své sídlo nebo místo
podnikání a nebyl stanoven zplnomocněný zástupce, udržuje
přístup k technické dokumentaci zdravotnického prostředku
osoba určená výrobcem podle § 12 odst. 4 nebo dovozce
podle přílohy č. I bodu 13.3.1. k tomuto nařízení.
Příl.VI
Ověřování shody zdravotnických prostředků s certifikovaným
typem zdravotnického prostředku na každém zdravotnickém
prostředku nebo statisticky vybraném vzorku
autorizovanou osobou
1. Ověřování shody zdravotnických prostředků s certifikovaným
typem zdravotnického prostředku podle volby výrobce nebo
dovozce na každém zdravotnickém prostředku nebo statisticky
vybraném vzorku autorizovanou osobou [§ 12 odst. 4 písm. f)
zákona] je postup, při kterém výrobce zajišťuje a prohlašuje,
že zdravotnické prostředky, které byly přezkoušeny
autorizovanou osobou podle bodu 4. této přílohy odpovídají
typu uvedenému v certifikátu o přezkoušení typu a vyhovují
ustanovením, která se na ně vztahují z tohoto nařízení.
2. Postup výrobce nebo dovozce.
2.1. Výrobce nebo dovozce provede nezbytná opatření, aby
zajistil, že vyráběné nebo dovážené zdravotnické
prostředky odpovídají typu uvedenému v certifikátu o
přezkoušení typu a vyhovují požadavkům, které se na ně
vztahují z tohoto nařízení,
2.2. výrobce připraví
2.2.1. výrobní proces, zejména pokud jde o sterilizaci,
jestliže je to nutné,
2.2.2. rutinní postupy s předběžnými opatřeními, která
mají být zavedena k zajištění stejnorodosti
výroby,
2.2.3. podle potřeby i soulad zdravotnických prostředků s
typem popsaným v certifikátu o přezkoušení typu a
s požadavky, které se na ně vztahují z tohoto
nařízení,
2.3. výrobce nebo dovozce postupuje v označování
zdravotnických prostředků v souladu s § 4 odst. 1 a
vypracuje písemné prohlášení o shodě,
2.4. výrobce zajišťuje a udržuje sterilitu při výrobě
zdravotnických prostředků uváděných na trh ve sterilním
stavu, za tím účelem postupuje kromě výše uvedeného i
podle bodů 3. a 4. přílohy č. VIII k tomuto nařízení.
3. Výrobce nebo dovozce poskytuje záruku, že zavede a bude
aktualizovat systematický postup získávání a vyhodnocování
informací a zkušeností uživatelů s těmito jím vyrobenými nebo
dovezenými zdravotnickými prostředky a v návaznosti na
uvedenou činnost provádět odpovídající nutná opatření, zejména
oznamovat vznik nežádoucích příhod, jakmile se o nich dozví.
4. Autorizovaná osoba
4.1. provede odpovídající přezkoumání a zkoušky k ověření
shody zdravotnického prostředku s požadavky tohoto
nařízení podle rozhodnutí výrobce nebo dovozce u
4.1.1. každého zdravotnického prostředku podle bodu 5.
této přílohy nebo
4.1.2. zdravotnických prostředků vybraných statisticky
podle bodu 6. této přílohy.
Uvedené přezkoumání a zkoušky neplatí pro požadavky na
výrobní proces, které jsou určeny pro zajištění
sterility.
5. Ověřování přezkoumáním a zkouškami každého zdravotnického
prostředku.
Autorizovaná osoba
5.1. zkouší každý zdravotnický prostředek individuálně, za
účelem ověření shody každého zdravotnického prostředku s
typem uvedeným v certifikátu o přezkoušení typu a s
požadavky, které se na ně vztahují z tohoto nařízení.
Autorizovaná osoba provádí odpovídající zkoušky stanovené
v příslušné normě (normách)8) a v případě potřeby provádí
ekvivalentní zkoušky,
5.2. umístí nebo nechá umístit na každý schválený zdravotnický
prostředek své identifikační číslo a s odvoláním na
provedené zkoušky vypracuje písemný certifikát o shodě
každého zdravotnického prostředku s typem uvedeným v
certifikátu o přezkoušení typu a s požadavky
vyplývajícími pro ně z tohoto nařízení.
6. Statistické ověřování.
6.1. Výrobce nebo dovozce předloží zdravotnické prostředky
vyrobené ve stejnorodých výrobních dávkách (šaržích).
6.2. Autorizovaná osoba odebere z každé výrobní dávky (šarže)
náhodně vybraný vzorek, jednotlivé zdravotnické
prostředky z tohoto vzorku zkoumá individuálně, přičemž
postupuje podle bodu 5.1. této přílohy.
6.3. Při statistické kontrole zdravotnických prostředků
autorizovaná osoba vychází z vlastností odběrového
systému, který zajišťuje mez jakosti odpovídající
pravděpodobnosti převzetí 5 % s hodnotou neshody mezi 3 %
a 7 %. Způsob odběru vzorků se stanoví podle
harmonizovaných norem8) a se zřetelem ke specifické
povaze kontrolovaných zdravotnických prostředků.
6.4. Jestliže autorizovaná osoba výrobní dávku (šarži)
převezme, umístí nebo nechá umístit na každý zdravotnický
prostředek své identifikační číslo a vypracuje písemný
certifikát o shodě s odvoláním na provedené zkoušky.
Všechny zdravotnické prostředky z výrobní dávky (šarže)
mohou být uvedeny na trh s výjimkou zdravotnických
prostředků ve vybraném vzorku, které byly shledány
nevyhovujícími.
Jestliže autorizovaná osoba výrobní dávku (šarži) odmítla
převzít, učiní přiměřená opatření, aby zabránila uvedení
výrobní dávky (šarže) na trh.
Autorizovaná osoba může pozastavit statistické ověřování,
v případě opakovaného odmítnutí převzetí výrobních dávek
(šarží).
Výrobce nebo dovozce může umisťovat na zdravotnický
prostředek identifikační číslo autorizované osoby na její
odpovědnost již v průběhu výrobního procesu.
7. Administrativní opatření.
Výrobce nebo dovozce uchovává a zpřístupňuje příslušným
orgánům státní správy po dobu nejméně 5 let po vyrobení
posledního zdravotnického prostředku
7.1. prohlášení o shodě,
7.2. dokumentaci uvedenou v bodu 2. této přílohy,
7.3. certifikáty uvedené v bodech 5.2. a 6.4. této přílohy a
7.4. certifikát o přezkoušení typu podle přílohy č. IV k
tomuto nařízení.
8. Použití u zdravotnických prostředků třídy IIa.
V souladu s § 8 odst. 2 lze tuto přílohu použít pro
zdravotnické prostředky třídy IIa s tím, že odchylně od
8.1. bodů 1. a 2. této přílohy na základě prohlášení o shodě
výrobce nebo dovozce zajišťuje a prohlašuje, že
zdravotnické prostředky třídy IIa jsou vyrobeny v souladu
s technickou dokumentací podle bodu 3. přílohy č. XII k
tomuto nařízení a vyhovují požadavkům, které se na ně
vztahují z tohoto nařízení,
8.2. bodů 1., 2., 5. a 6. této přílohy jsou ověření provedená
autorizovanou osobou určena k potvrzení shody
zdravotnických prostředků třídy IIa s technickou
dokumentací podle bodu 3. přílohy č. XII k tomuto
nařízení.
------------------------------------------------------------------
8) § 4a odst. 1 zákona č. 22/1997 Sb., o technických požadavcích
na výrobky a o změně a doplnění některých zákonů, ve znění
zákona č. 71/2000 Sb.
Příl.VII
ES ověřování
1. ES ověřování je postup, kterým výrobce nebo jeho zplnomocněný
zástupce zajišťuje a prohlašuje, že zdravotnické prostředky,
které byly přezkoušeny autorizovanou osobou podle bodu 4. této
přílohy, odpovídají typu uvedenému v ES certifikátu o
přezkoušení typu a vyhovují ustanovením, která se na ně
vztahují z tohoto nařízení.
2. Postup výrobce.
Výrobce
2.1. provede nezbytná opatření, aby zajistil, že vyráběné
zdravotnické prostředky odpovídají typu uvedenému v ES
certifikátu o přezkoušení typu a vyhovují požadavkům,
které se na ně vztahují z tohoto nařízení,
2.2. připraví, před zahájením výroby, dokumenty vymezující
2.2.1. výrobní proces, zejména pokud jde o sterilizaci,
jestliže je to nutné,
2.2.2. rutinní postupy s předběžnými opatřeními, která
mají být zavedena k zajištění stejnorodosti
výroby,
2.2.3. podle potřeby i soulad zdravotnických prostředků s
typem uvedeným v ES certifikátu o přezkoušení typu
a s požadavky, které se na ně vztahují z tohoto
nařízení,
2.3. připojí označení CE v souladu s § 4 a vypracuje písemné
prohlášení o shodě,
2.4. zajišťuje a udržuje sterilitu při výrobě zdravotnických
prostředků uváděných na trh ve sterilním stavu, za tím
účelem postupuje kromě výše uvedeného i podle bodů 3. a
4. přílohy č. VIII k tomuto nařízení.
3. Výrobce poskytuje záruku, že zavede a bude aktualizovat
systematický postup získávání a vyhodnocování informací a
zkušeností uživatelů s těmito jím vyrobenými zdravotnickými
prostředky a v návaznosti na uvedenou činnost provádět
odpovídající nutná opatření, zejména oznamovat vznik
nežádoucích příhod, jakmile se o nich dozví.
4. Autorizovaná osoba
4.1. provede odpovídající přezkoumání a zkoušky k ověření
shody zdravotnického prostředku s požadavky tohoto
nařízení podle rozhodnutí výrobce u
4.1.1. každého zdravotnického prostředku podle bodu 5.
této přílohy nebo
4.1.2. zdravotnických prostředků vybraných statisticky
podle bodu 6. této přílohy.
Uvedené kontroly neplatí pro hlediska výrobního postupu,
která jsou určena pro zajištění sterility.
5. Ověřování přezkoumáním a zkouškami každého zdravotnického
prostředku.
Autorizovaná osoba
5.1. zkouší každý zdravotnický prostředek individuálně, za
účelem ověření shody každého zdravotnického prostředku s
typem uvedeným v ES certifikátu o přezkoušení typu a s
požadavky, které se na ně vztahují z tohoto nařízení.
Autorizovaná osoba provádí odpovídající zkoušky stanovené
v příslušné normě (normách)8) a v případě potřeby provádí
ekvivalentní zkoušky,
5.2. umístí nebo nechá umístit na každý schválený zdravotnický
prostředek své identifikační číslo a s odvoláním na
provedené zkoušky vypracuje písemný certifikát o shodě
každého zdravotnického prostředku s typem uvedeným v ES
certifikátu o přezkoušení typu a s požadavky
vyplývajícími pro ně z tohoto nařízení.
6. Statistické ověřování.
6.1. Výrobce předloží zdravotnické prostředky vyrobené ve
stejnorodých výrobních dávkách (šaržích).
6.2. Autorizovaná osoba odebere z každé výrobní dávky (šarže)
náhodně vybraný vzorek, jednotlivé zdravotnické
prostředky z tohoto vzorku zkoumá individuálně, přičemž
postupuje podle bodu 5. této přílohy.
6.3. Při statistické kontrole zdravotnických prostředků
autorizovaná osoba vychází z vlastností odběrového
systému, který zajišťuje mez jakosti odpovídající
pravděpodobnosti převzetí 5 % s hodnotou neshody mezi 3 %
a 7 %. Způsob odběru vzorků se stanoví podle
harmonizovaných norem8) a se zřetelem ke specifické
povaze kontrolovaných zdravotnických prostředků.
6.4. Jestliže autorizovaná osoba výrobní dávku (šarži)
převezme, umístí nebo nechá umístit na každý zdravotnický
prostředek své identifikační číslo a vypracuje písemný
certifikát o shodě s odvoláním na provedené zkoušky.
Všechny zdravotnické prostředky z výrobní dávky (šarže)
mohou být uvedeny na trh s výjimkou zdravotnických
prostředků ve vybraném vzorku, které byly shledány
nevyhovujícími.
Jestliže autorizovaná osoba výrobní dávku (šarži) odmítla
převzít, učiní opatření, aby zabránila uvedení výrobní
dávky (šarže) na trh.
Autorizovaná osoba může pozastavit statistické ověřování,
v případě častého odmítnutí převzetí výrobních dávek
(šarží).
Výrobce může umisťovat na zdravotnický prostředek
identifikační číslo autorizované osoby na její
odpovědnost již v průběhu výrobního procesu.
7. Administrativní opatření.
Výrobce nebo jeho zmocněný zástupce uchovává a zpřístupňuje
příslušným orgánům státní správy po dobu nejméně 5 let po
vyrobení posledního zdravotnického prostředku
7.1. prohlášení o shodě,
7.2. dokumentaci uvedenou v bodu 2. této přílohy,
7.3. ES certifikáty uvedené v bodech 5.2. a 6.4. této přílohy
a
7.4. ES certifikát o přezkoušení typu podle přílohy č. V k
tomuto nařízení.
8. Použití u zdravotnických prostředků třídy IIa.
V souladu s § 9 odst. 2 lze tuto přílohu použít pro
zdravotnické prostředky třídy IIa s tím, že odchylně od
8.1. bodů 1. a 2. této přílohy na základě prohlášení o shodě
výrobce zajišťuje a prohlašuje, že zdravotnické
prostředky třídy IIa jsou vyrobeny v souladu s technickou
dokumentací podle bodu 3. přílohy č. XIII k tomuto
nařízení a vyhovují požadavkům, které se na ně vztahují z
tohoto nařízení,
8.2. bodů 1., 2., 5. a 6. této přílohy jsou ověření provedená
autorizovanou osobou určena k potvrzení shody
zdravotnických prostředků třídy IIa s technickou
dokumentací podle bodu 3. přílohy č. XIII k tomuto
nařízení.
------------------------------------------------------------------
8) § 4a odst. 1 zákona č. 22/1997 Sb., o technických požadavcích
na výrobky a o změně a doplnění některých zákonů, ve znění
zákona č. 71/2000 Sb.
Příl.VIII
Posouzení systému jakosti výroby
(Zabezpečení jakosti výroby)
1. Posouzení systému jakosti výroby u výrobce autorizovanou
osobou [§ 12 odst. 4 písm. d) zákona] je postup, při kterém
autorizovaná osoba posuzuje systém jakosti schválený pro
výrobu příslušných zdravotnických prostředků a provádění
výstupní kontroly podle bodu 3. této přílohy, přičemž
a) výrobce postupující podle bodu 2. nebo
b) dovozce postupující podle bodu 2a.
zaručuje a prohlašuje, že příslušné zdravotnické prostředky
odpovídají typu popsanému v certifikátu o přezkoušení typu a
vyhovují ustanovením, která se na ně vztahují z tohoto
nařízení.
2. Výrobce
2.1. zajišťuje uplatňování systému jakosti schváleného pro
výrobu příslušných zdravotnických prostředků,
2.2. provádí výstupní kontrolu bodu 3.,
2.3. postupuje v označování zdravotnických prostředků v
souladu s § 4 odst. 1,
2.4. vypracuje a uchovává písemné prohlášení o shodě, které
musí zahrnovat vyrobený počet identifikovaných vzorků
zdravotnických prostředků,
2.5. podléhá dozoru příslušné autorizované osoby podle bodu 4.
této přílohy.
2a. Dovozce
2a.1. postupuje v označování zdravotnických prostředků v
souladu s § 4 odst. 1,
2a.2. vypracuje a uchovává písemné prohlášení o shodě, které
musí zahrnovat vyrobený počet identifikovaných vzorků
zdravotnických prostředků.
3. Systém jakosti.
3.1. Výrobce nebo dovozce
3.1.1. předkládá písemnou žádost autorizované osobě o
posouzení (vyhodnocení a schválení) svého systému
jakosti; žádost musí obsahovat
3.1.1.1. jméno, příjmení, adresu trvalého pobytu a
místa podnikání výrobce, jestliže jde o
fyzickou osobu; název (obchodní firmu),
adresu sídla a místa podnikání, je-li
výrobcem právnická osoba,
3.1.1.2. významné informace o zdravotnickém
prostředku, pro který platí postup
uvedený v bodu 1.,
3.1.1.3. písemné prohlášení, že u jiné
autorizované osoby nebyla podána žádost o
posouzení systému jakosti výroby
vztahující se ke stejnému zdravotnickému
prostředku,
3.1.1.4. dokumentaci systému jakosti,
3.1.1.5. záruku výrobce plnit požadavky
vyplývající ze schváleného systému
jakosti,
3.1.1.6. záruku výrobce udržovat schválený systém
jakosti v použitelném a účinném stavu,
3.1.1.7. v případě potřeby technickou dokumentaci
schválených typů zdravotnických
prostředků a kopii certifikátu o
přezkoušení typu,
3.1.1.8. záruku výrobce, že zavede a bude
aktualizovat systematický postup
získávání a vyhodnocování informací a
zkušeností uživatelů s jím vyrobenými
zdravotnickými prostředky a v návaznosti
na uvedenou činnost provádět odpovídající
nápravná opatření, zejména oznamovat
vznik nežádoucích příhod, jakmile se o
nich dozví.
3.2. Uplatnění systému jakosti musí zajistit, že vyrobené
zdravotnické prostředky odpovídají typu popsanému v
certifikátu o přezkoušení typu.
Prvky a požadavky schválené výrobcem pro systém jakosti
musí být systematicky a řádně dokumentovány v písemně
vypracovaných zásadách a postupech. Tato dokumentace
systému jakosti musí umožnit jednotný výklad koncepce
jakosti zdravotnických prostředků a postupů, zejména
programů jakosti, plánů jakosti, příruček jakosti
a záznamů o jakosti.
Dokumentace systému jakosti musí obsahovat zejména popis
3.2.1. cílů jakosti u výrobce,
3.2.2. organizace výrobce, zejména
3.2.2.1. organizačních struktur, zodpovědnosti
vedoucích zaměstnanců a jejich pravomocí
ve vztahu k výrobě zdravotnických
prostředků,
3.2.2.2. metod sledování účinnosti systému
jakosti, zejména jeho schopnosti
dosáhnout požadované jakosti
zdravotnického prostředku, včetně
kontroly zdravotnických prostředků, které
požadované jakosti nedosáhnou,
3.2.3. techniky kontrol a zajištění jakosti
zdravotnických prostředků ve stadiu jejich výroby,
zejména
3.2.3.1. postupy, které budou použity především
pokud jde o sterilizaci, prodej a
příslušné dokumenty,
3.2.3.2. postupy k identifikaci zdravotnického
prostředku vypracované a aktualizované ke
všem stadiím výroby na základě výkresů,
specifikací a dalších odpovídajících
dokumentů,
3.2.4. příslušné testy a zkoušky, které budou vykonány
před výrobou, během výroby a po výrobě
zdravotnických prostředků, jejich četnost a
použitá zkušební zařízení; zpětně musí být možné
přiměřeným způsobem zjistit správnost kalibrace
zkušebních zařízení.
3.3. Autorizovaná osoba provádí audity systému jakosti za
účelem zjištění, zda systém jakosti vyhovuje požadavkům
uvedeným v bodu 3.2. této přílohy. Shoda s těmito
požadavky se předpokládá u systémů jakosti, u kterých se
používají odpovídají normy.
V týmu pověřeném hodnocením systému jakosti musí být
alespoň jeden člen, který má zkušenosti s hodnocením
příslušných technologií. Hodnotitelský postup zahrnuje
prohlídku provozních prostor výrobce a v odůvodněných
případech i kontrolu výrobních postupů v provozních
prostorech dodavatelů výrobce, popřípadě jeho dalších
smluvních stran.
Po provedeném auditu systému jakosti autorizovaná osoba
oznámí výrobci nebo dovozci rozhodnutí, které musí
obsahovat závěry kontroly a odůvodněné zhodnocení.
3.4. Výrobce nebo dovozce informuje autorizovanou osobu, která
schválila systém jakosti, o záměru, který podstatně mění
systém jakosti nebo jím pokrytý okruh zdravotnických
prostředků.
Autorizovaná osoba zhodnotí navrhované změny, ověří, zda
takto změněný systém jakosti ještě vyhovuje požadavkům
uvedeným v bodu 3.2. této přílohy a oznámí výrobci nebo
dovozci své rozhodnutí, které musí obsahovat závěry
kontroly a odůvodněné zhodnocení.
4. Dozor.
4.1. Cílem dozoru je zajistit, aby výrobce náležitě plnil
požadavky vyplývající ze schváleného systému jakosti.
4.2. Za účelem uvedeným v bodu 4.1. této přílohy výrobce
zmocňuje autorizovanou osobu k provádění nezbytných
kontrol a poskytuje jí příslušné informace, zejména
4.2.1. dokumentaci systému jakosti,
4.2.2. údaje vymezené systémem jakosti pro oblast výroby
zdravotnických prostředků, především kontrolní
zprávy, údaje o zkouškách, kalibraci a zprávy o
kvalifikaci příslušných zaměstnanců.
4.3. Autorizovaná osoba provádí
4.3.1. periodicky příslušné kontroly a hodnocení tak, aby
se ujistila, že výrobce používá schválený systém
jakosti, výrobci poskytuje o provedené kontrole
hodnotící zprávu,
4.3.2. podle svého uvážení u výrobce i předem neohlášené
kontroly, při nichž v případě potřeby provede nebo
nechá provést zkoušky za účelem kontroly, zda
systém jakosti je řádně činný; o provedené
kontrole, popřípadě i o výsledku provedené
zkoušky, poskytuje výrobci písemnou zprávu.
5. Administrativní opatření.
5.1. Výrobce nebo dovozce uchovává a zpřístupňuje příslušným
orgánům státní správy
5.1.1. prohlášení o shodě,
5.1.2. dokumentaci systému jakosti,
5.1.3. změny podle bodu 3.4. této přílohy,
5.1.4. v případě potřeby technickou dokumentaci
schválených typů a kopie certifikátů o přezkoušení
typu,
5.1.5. rozhodnutí a zprávy autorizované osoby podle bodů
3.4. a 4.3. této přílohy,
5.1.6. certifikát o přezkoušení typu podle přílohy č. IV
k tomuto nařízení,
a to po dobu nejméně 5 let po vyrobení posledního
zdravotnického prostředku.
6. Použití pro zdravotnické prostředky třídy IIa.
6.1. V souladu s § 8 odst. 2 lze tuto přílohu použít pro
zdravotnické prostředky třídy IIa s tím, že odchylně od
bodů 1., 2., 2a., 3.1. a 3.2. této přílohy výrobce nebo
dovozce na základě prohlášení o shodě zajišťuje a
prohlašuje, že zdravotnické prostředky třídy IIa jsou
vyrobeny ve shodě s technickou dokumentací podle bodu 3.
přílohy č. XII k tomuto nařízení a vyhovují požadavkům,
které se na ně vztahují z tohoto nařízení.
Příl.IX
ES prohlašování o shodě
(Zabezpečení jakosti výroby)
1. ES prohlašování o shodě (Zabezpečení jakosti výroby) je částí
postupu, kterým výrobce plnící požadavky podle bodu 2.1.1. až
2.4. zaručuje a prohlašuje, že příslušné zdravotnické
prostředky odpovídají typu uvedenému v ES certifikátu o
přezkoušení typu a vyhovují ustanovením, která se na ně
vztahují z tohoto nařízení.
2. Výrobce
2.1. zajišťuje uplatňování systému jakosti schváleného pro
výrobu příslušných zdravotnických prostředků,
2.2. provádí výstupní kontrolu podle bodu 3.,
2.3. označuje zdravotnické prostředky v souladu s § 4 odst. 2,
2.4. vypracuje a uchovává písemné prohlášení o shodě, které
musí zahrnovat příslušný počet identifikovaných vzorků
vyrobených zdravotnických prostředků a
2.5. podléhá dozoru příslušné autorizované osoby podle bodu 4.
této přílohy.
3. Systém jakosti.
3.1. Výrobce
3.1.1. předkládá písemnou žádost autorizované osobě o
posouzení (vyhodnocení a schválení) svého systému
jakosti; žádost musí obsahovat
3.1.1.1. jméno, příjmení a adresu trvalého pobytu
výrobce, jestliže jde o fyzickou osobu;
název (obchodní firmu) a adresu sídla,
jestliže jde o právnickou osobu,
3.1.1.2. v případě potřeby technickou dokumentaci
schválených typů zdravotnických
prostředků a kopii ES certifikátu o
přezkoušení typu,
3.1.1.3. náležitosti uvedené v bodech 3.1.1.3. až
3.1.1.8. přílohy č. VIII k tomuto
nařízení.
3.2. Uplatnění systému jakosti musí zajistit, že vyrobené
zdravotnické prostředky odpovídají typu uvedenému v ES
certifikátu o přezkoušení typu.
Prvky, ustanovení a požadavky schválené výrobcem pro
systém jakosti musí být systematicky a řádně
dokumentovány v písemně vypracovaných zásadách a
postupech. Tato dokumentace systému jakosti musí umožnit
jednotný výklad koncepce jakosti zdravotnických
prostředků a postupů, zejména programů jakosti, plánů
jakosti, příruček jakosti a záznamů o jakosti.
3.2.1. Dokumentace systému jakosti musí obsahovat zejména
popis požadavků uvedených v bodech 3.2.1. až
3.2.4. přílohy č. VIII k tomuto nařízení.
3.3. Pro audity systému jakosti platí ustanovení bodu 3.3.
přílohy č. VIII k tomuto nařízení.
3.4. Činnost výrobce a autorizované osoby týkající se změn
systému jakosti se řídí podle bodu 3.4. přílohy č. VIII k
tomuto nařízení.
4. Pro dozor platí ustanovení bodu 4. přílohy č. VIII k tomuto
nařízení.
5. Administrativní opatření.
5.1. Výrobce uchovává a zpřístupňuje příslušným orgánům státní
správy
5.1.1. prohlášení o shodě,
5.1.2. dokumentaci systému jakosti,
5.1.3. změny podle bodu 3.4. přílohy č. VIII k tomuto
nařízení,
5.1.4. technickou dokumentaci schválených typů a kopie ES
certifikátů o přezkoušení typu,
5.1.5. rozhodnutí a zprávy autorizované osoby podle bodů
3.4. a 4.3. přílohy č. VIII k tomuto nařízení,
5.1.6. ES certifikát o přezkoušení typu podle přílohy č.
V k tomuto nařízení,
a to po dobu nejméně 5 let po vyrobení posledního
zdravotnického prostředku.
6. Použití pro zdravotnické prostředky třídy IIa.
6.1. V souladu s § 9 odst. 2 lze tuto přílohu použít pro
zdravotnické prostředky třídy IIa s tím, že odchylně od
bodů 1., 2., 3.1. a 3.2. této přílohy výrobce na základě
prohlášení o shodě zajišťuje a prohlašuje, že
zdravotnické prostředky třídy IIa jsou vyrobeny ve shodě
s technickou dokumentací podle bodu 3. přílohy č. XIII k
tomuto nařízení a vyhovují požadavkům, které se na ně
vztahují z tohoto nařízení.
Příl.X
Posouzení systému jakosti zdravotnických prostředků
(Zabezpečení jakosti zdravotnických prostředků)
1. Posouzení systému jakosti zdravotnických prostředků
autorizovanou osobou [§ 12 odst. 4 písm. e) zákona] je postup,
při kterém autorizovaná osoba posuzuje systém jakosti
provozovaný výrobcem podle bodu 3. této přílohy a výrobce
plnící požadavky podle bodu 2. a 2a. této přílohy nebo dovozce
plnící požadavky podle bodu 2a. této přílohy zaručuje a
prohlašuje, že příslušné zdravotnické prostředky odpovídají
typu popsanému v certifikátu o přezkoušení typu a vyhovují
ustanovením, která se na ně vztahují z tohoto nařízení.
2. Výrobce
2.1. zajišťuje uplatňování systému jakosti schváleného pro
výstupní kontrolu a zkoušení zdravotnických prostředků
podle bodu 3. této přílohy,
2.2. zajišťuje a udržuje sterilitu při výrobě zdravotnických
prostředků uváděných na trh ve sterilním stavu, za tím
účelem postupuje podle přílohy č. VIII bodů 3. a 4.
k tomuto nařízení a
2.3. podléhá dozoru příslušné autorizované osoby podle bodu 4.
této přílohy.
2a. Výrobce nebo dovozce
2a.1. postupuje v označování zdravotnických prostředků v
souladu s § 4 odst. 1, k označení připojuje
identifikační číslo autorizované osoby, která plní úkoly
podle této přílohy a
2a.2. vypracuje a uchovává písemné prohlášení o shodě, které
musí obsahovat náležitosti uvedené v § 14 a musí
zahrnovat počet identifikovaných vzorků vyrobených
zdravotnických prostředků.
3. Systém jakosti.
3.1. Výrobce nebo dovozce
3.1.1. předkládá písemnou žádost autorizované osobě o
posouzení (vyhodnocení a schválení) svého systému
jakosti; žádost musí obsahovat
3.1.1.1. jméno, příjmení, adresu trvalého pobytu a
místa podnikání výrobce, jestliže jde o
fyzickou osobu, název (obchodní firmu),
adresu sídla a místa podnikání, je-li
výrobcem právnická osoba,
3.1.1.2. potřebné informace o zdravotnickém
prostředku nebo o kategorii
zdravotnických prostředků, pro které
platí postup uvedený v bodu 1.,
3.1.1.3. písemné prohlášení, že u jiné
autorizované osoby nebyla podána žádost o
posouzení systému jakosti pro stejné
zdravotnické prostředky,
3.1.1.4. dokumentaci systému jakosti,
3.1.1.5. záruku výrobce plnit požadavky
vyplývající ze schváleného systému
jakosti,
3.1.1.6. záruku výrobce udržovat schválený systém
jakosti na odpovídající a efektivní
úrovni,
3.1.1.7. v případě potřeby technickou dokumentaci
schválených typů a kopii certifikátu o
přezkoušení typu,
3.1.1.8. záruku výrobce, že zavede a bude
aktualizovat systematický postup
získávání a vyhodnocování informací a
zkušeností uživatelů s těmito jím
vyrobenými zdravotnickými prostředky a v
návaznosti na uvedenou činnost provádět
odpovídající nápravná opatření, zejména
oznamovat vznik nežádoucích příhod,
jakmile se o nich dozví.
3.2. Výrobce v rámci tohoto systému jakosti
3.2.1. přezkoumá každý zdravotnický prostředek nebo
reprezentativní vzorek z každé výrobní dávky
(šarže),
3.2.2. provede příslušné zkoušky stanovené v odpovídající
normě (normách),8) popřípadě ekvivalentní zkoušky,
aby se ujistil, že zdravotnické prostředky
odpovídají typu popsanému v certifikátu o
přezkoušení typu nebo v ES certifikátu o
přezkoušení typu pokud výrobce postupoval podle
§ 9 a vyhovují ustanovením, která se na ně
vztahují z tohoto nařízení,
3.2.3. systematicky a řádně dokumentuje prvky, požadavky
a ustanovení jím přijaté formou písemných
opatření, postupů a pokynů; tato dokumentace musí
umožnit jednotný výklad programu jakosti, plánu
jakosti, příruček jakosti a záznamů o jakosti.
Tato dokumentace musí zahrnovat zejména
odpovídající popis
3.2.3.1. cílů jakosti u výrobce,
3.2.3.2. organizačních struktur, odpovědnosti a
pravomoci vedoucích zaměstnanců z
hlediska jakosti výroby,
3.2.3.3. přezkoumání a zkoušek zdravotnických
prostředků po jejich vyrobení; zpětně
musí být možné přiměřeným způsobem
zjistit správnost kalibrace zkušebních
zařízení,
3.2.3.4. metod sledování účinnosti systému
jakosti,
3.2.3.5. záznamů o jakosti, především kontrolních
zpráv, zpráv o zkouškách a kalibraci
a o kvalifikaci příslušných zaměstnanců.
Uvedené kontroly neplatí pro oblasti výrobního
procesu určené k zajištění sterility.
3.3. Autorizovaná osoba
3.3.1. provádí audity systému jakosti u výrobce s cílem
zjistit, zda tento systém vyhovuje požadavkům
podle bodu 3.2. této přílohy, shodu s těmito
požadavky předpokládá u systémů jakosti, ve
kterých se používají harmonizované normy.8)
V týmu pověřeném hodnocením systému jakosti musí
být alespoň jeden člen, který má zkušenosti s
hodnocením příslušných technologií. Hodnotitelský
postup zahrnuje kontrolu provozních prostor
výrobce a v odůvodněných případech i kontrolu
výrobních postupů v provozních prostorech
dodavatelů výrobce.
Po provedeném auditu systému jakosti autorizovaná
osoba oznámí výrobci rozhodnutí, které musí
obsahovat závěry z provedeného auditu a jejich
odůvodněné zhodnocení.
3.4. Výrobce nebo dovozce informuje autorizovanou osobu, která
schválila systém jakosti, o záměru, kterým se podstatně
mění tento systém.
Autorizovaná osoba zhodnotí navrhované změny a ověří, zda
takto změněný systém jakosti ještě vyhovuje požadavkům
uvedeným v bodu 3.2. této přílohy a oznámí své rozhodnutí
výrobci; toto rozhodnutí musí obsahovat závěry kontroly a
odůvodněné zhodnocení.
4. Dozor.
4.1. Cílem dozoru je zajistit, aby výrobce náležitě plnil
požadavky vyplývající ze schváleného systému jakosti.
4.2. Za účelem uvedeným v bodu 4.1. této přílohy výrobce
4.2.1. umožňuje autorizované osobě přístup do
kontrolních, zkušebních a skladovacích prostorů,
které používá v rámci výroby zdravotnických
prostředků,
4.2.2. poskytuje autorizované osobě příslušné informace,
zejména
4.2.2.1. dokumentaci systému jakosti,
4.2.2.2. technickou dokumentaci,
4.2.2.3. záznamy o jakosti, především kontrolní
zprávy, údaje o zkouškách a kalibraci a o
kvalifikaci příslušných zaměstnanců.
4.3. Autorizovaná osoba
4.3.1. provádí periodicky příslušné kontroly a hodnocení
tak, aby se ujistila, že výrobce používá schválený
systém jakosti a
4.3.2. poskytuje výrobci hodnotící zprávu.
4.4. Autorizovaná osoba provádí u výrobce podle svého uvážení
i předem neohlášené kontroly, při nichž v případě potřeby
provede nebo si vyžádá provedení zkoušky za účelem
kontroly, zda systém jakosti je řádně činný a výroba
zdravotnických prostředků odpovídá požadavkům, které se
na ně vztahují z tohoto nařízení.
Při těchto kontrolách se ověřuje odpovídající vzorek
vyrobených zdravotnických prostředků odebraný u výrobce
autorizovanou osobou a provedou se příslušné zkoušky
podle odpovídajících norem8) nebo v případě potřeby se
provádí zkoušky ekvivalentní. Jestliže se neshoduje jeden
nebo více vzorků, učiní autorizovaná osoba příslušná
opatření.
Autorizovaná osoba poskytne výrobci zprávu o kontrole a
jestliže byly provedeny zkoušky i zkušební zprávu.
5. Administrativní opatření.
5.1. Výrobce nebo dovozce uchovává a zpřístupňuje pro potřebu
příslušných orgánů státní správy po dobu nejméně 5 let po
vyrobení posledního zdravotnického prostředku
5.1.1. prohlášení o shodě,
5.1.2. technickou dokumentaci schválených typů
zdravotnických prostředků a kopii certifikátu o
přezkoušení typu,
5.1.3. změny podle bodu 3.4. této přílohy,
5.1.4. rozhodnutí a zprávy autorizované osoby podle bodu
3.4. této přílohy a bodů 4.3. a 4.4. této přílohy,
5.1.5. podle okolností certifikát o shodě podle přílohy
č. IV k tomuto nařízení.
6. Použití pro zdravotnické prostředky třídy IIa.
V souladu s § 8 odst. 2 lze tuto přílohu použít pro
zdravotnické prostředky třídy IIa s tím, že odchylně od bodů
2., 2a., 3.1. a 3.2. této přílohy výrobce nebo dovozce na
základě prohlášení o shodě zajišťuje a prohlašuje, že
zdravotnické prostředky třídy IIa jsou vyrobeny ve shodě s
technickou dokumentací podle bodu 3 přílohy č. XII k tomuto
nařízení a vyhovují požadavkům, které se na ně vztahují z
tohoto nařízení.
------------------------------------------------------------------
8) § 4a odst. 1 zákona č. 22/1997 Sb., o technických požadavcích
na výrobky a o změně a doplnění některých zákonů, ve znění
zákona č. 71/2000 Sb.
Příl.XI
ES prohlašování o shodě
(Zabezpečení jakosti zdravotnického prostředku)
1. ES prohlašování s shodě je součástí postupu, kterým výrobce
plnící požadavky podle bodu 2. zaručuje a prohlašuje, že
příslušné zdravotnické prostředky odpovídají typu uvedenému v
ES certifikátu o přezkoušení typu a vyhovují ustanovením,
která se na ně vztahují z tohoto nařízení.
2. Výrobce
2.1. zajišťuje uplatňování systému jakosti schváleného pro
výstupní kontrolu a zkoušení zdravotnických prostředků
podle bodu 3.,
2.2. zajišťuje a udržuje sterilitu při výrobě zdravotnických
prostředků uváděných na trh ve sterilním stavu, za tím
účelem postupuje podle přílohy č. IX bodů 3. a 4.
k tomuto nařízení,
2.3. označuje zdravotnické prostředky v souladu s § 4 odst. 2
a k označení připojuje identifikační číslo autorizované
osoby, která plní úkoly podle této přílohy,
2.4. vypracuje a uchovává písemné prohlášení o shodě, které
musí zahrnovat počet identifikovaných vzorků vyrobených
zdravotnických prostředků,
2.5. podléhá dozoru příslušné autorizované osoby podle bodu 4.
této přílohy.
3. V systému jakosti plní
a) výrobce úkoly uvedené v bodech 3.1. a 3.2. přílohy č. X k
tomuto nařízení,
b) autorizovaná osoba úkoly uvedené v bodu 3.3. a 3.4. přílohy
č. X k tomuto nařízení.
4. Při dozoru se postupuje podle bodu 4. přílohy č. X k tomuto
nařízení.
5. Administrativní opatření.
5.1. Výrobce uchovává a zpřístupňuje pro potřebu příslušných
orgánů státní správy po dobu nejméně 5 let po vyrobení
posledního zdravotnického prostředku
5.1.1. prohlášení o shodě,
5.1.2. technickou dokumentaci schválených typů
zdravotnických prostředků a kopii ES certifikátu o
přezkoušení typu,
5.1.3. změny podle přílohy č. X bodu 3.4. k tomuto
nařízení,
5.1.4. rozhodnutí a zprávy autorizované osoby podle
přílohy č. X bodu 4.3. a 4.4. k tomuto nařízení,
5.1.5. podle okolností certifikát o shodě podle přílohy
č. V k tomuto nařízení.
6. Použití pro zdravotnické prostředky třídy IIa.
V souladu s § 9 odst. 2 lze tuto přílohu použít pro
zdravotnické prostředky třídy IIa s tím, že odchylně od bodu
2. této přílohy a bodů 3.1. a 3.2. přílohy č. X k tomuto
nařízení výrobce na základě prohlášení o shodě zajišťuje a
prohlašuje, že zdravotnické prostředky třídy IIa jsou vyrobeny
ve shodě s technickou dokumentací podle bodu 3. přílohy č.
XIII k tomuto nařízení a vyhovují požadavkům, které se na ně
vztahují z tohoto nařízení.
Příl.XII
Posouzení shody za stanovených podmínek
výrobcem nebo dovozcem
1. Posouzení shody za stanovených podmínek výrobcem nebo dovozcem
[§ 12 odst. 4 písm. a) zákona] je postup, při kterém výrobce
nebo dovozce plnící požadavky podle bodu 2. této přílohy a v
případě zdravotnických prostředků uváděných na trh ve
sterilním stavu a zdravotnických prostředků s měřicí funkcí
plní i požadavky uvedené v bodě 5. této přílohy, posuzuje
shodu zdravotnického prostředku s požadavky tohoto nařízení a
jestliže zjistil shodu zaručuje a prohlašuje, že zdravotnické
prostředky vyhovují ustanovením, která se na ně vztahují z
tohoto nařízení.
2. Výrobce nebo dovozce připraví technickou dokumentaci podle
bodu 3. této přílohy a zpřístupňuje tuto dokumentaci, včetně
prohlášení o shodě, příslušným orgánům státní správy pro
kontrolní účely po dobu nejméně 5 let po vyrobení posledního
zdravotnického prostředku. Není-li ustanoven ani výrobce ani
dovozce, udržuje přístup k technické dokumentaci osoba, která
uvedla nebo uvádí v České republice zdravotnický prostředek na
trh.
3. Technická dokumentace musí umožnit hodnocení shody
zdravotnického prostředku s požadavky tohoto nařízení; tato
dokumentace musí obsahovat zejména
3.1. všeobecný popis typu, včetně zamýšlených variant,
3.2. konstrukční výkresy, připravované výrobní technologie a
schémata částí, podsestav, popřípadě obvodů,
3.3. popisy a vysvětlení nezbytné k porozumění výše uvedeným
výkresům, schématům a funkci zdravotnického prostředku,
3.4. výsledky analýzy rizik a seznam norem,8) které byly úplně
nebo částečně použity, a popisy řešení schválených pro
splnění základních požadavků, pokud normy8) nebyly
použity v plném rozsahu,
3.5. popis použitých metod sterilizace u zdravotnických
prostředků uváděných na trh ve sterilním stavu,
3.6. výsledky zejména konstrukčních výpočtů a provedených
kontrol; jestliže ke splnění určeného účelu použití má
být zdravotnický prostředek spojen s jinými
zdravotnickými prostředky, musí být prokázáno, že
zdravotnický prostředek vyhovuje základním požadavkům při
spojení se zdravotnickým prostředkem nebo zdravotnickými
prostředky, který má (mají) charakteristiky specifikované
výrobcem nebo dovozcem,
3.7. zkušební zprávy, popřípadě klinické údaje získané podle
přílohy č. XVII k tomuto nařízení a
3.8. návod k použití zdravotnického prostředku a návrh
označení zdravotnického prostředku ve smyslu § 4 odst. 1.
4. Výrobce nebo dovozce zavede a aktualizuje systematický postup
získávání a vyhodnocování informací a zkušeností uživatelů s
těmito jím vyrobenými nebo dovezenými zdravotnickými
prostředky a v návaznosti na uvedenou činnost provede
odpovídající nápravná opatření, zejména oznamovat vznik
nežádoucích příhod, jakmile se o nich dozví.
5. U zdravotnických prostředků uváděných na trh ve sterilním
stavu a u zdravotnických prostředků třídy I s měřicí funkcí
výrobce nebo dovozce dodržuje kromě ustanovení této přílohy i
jeden z postupů podle příloh č. VI, VIII nebo X k tomuto
nařízení. Použití uvedených příloh a opatření autorizované
osoby se omezuje u zdravotnických prostředků
5.1. uváděných na trh ve sterilním stavu pouze na výrobní
hlediska, která se dotýkají zajišťování a udržování
sterilních podmínek,
5.2. s měřicí funkcí pouze na výrobní hlediska, která
souvisejí se shodou těchto prostředků s metrologickými
požadavky,
přičemž lze použít ustanovení bodu 6.1. této přílohy.
6. Použití pro prostředky třídy IIa.
6.1. V souladu s § 8 odst. 2 může být tato příloha použita pro
zdravotnické prostředky třídy IIa s tím, že při použití
této přílohy ve spojení s postupem podle příloh č. VI,
VIII nebo X k tomuto nařízení tvoří prohlášení o shodě
podle uvedených příloh jediné prohlášení. Prohlášení,
které vychází z této přílohy výrobce nebo dovozce
zaručuje a prohlašuje, že návrh zdravotnického prostředku
vyhovuje ustanovením, která se na něj vztahují z tohoto
nařízení.
------------------------------------------------------------------
8) § 4a odst. 1 zákona č. 22/1997 Sb., o technických požadavcích
na výrobky a o změně a doplnění některých zákonů, ve znění
zákona č. 71/2000 Sb.
Příl.XIII
ES prohlašování o shodě
1. ES prohlašování o shodě je postup, kterým výrobce nebo jeho
zplnomocněný zástupce plnící požadavky podle bodu 2. a v
případě zdravotnických prostředků uváděných na trh ve
sterilním stavu a zdravotnických prostředků s měřicí funkcí
požadavky podle bodu 5. této přílohy, zaručuje a prohlašuje,
že zdravotnické prostředky vyhovují ustanovením, která se na
ně vztahují z tohoto nařízení.
2. Výrobce připraví technickou dokumentaci podle bodu 3. této
přílohy. Výrobce nebo jeho zplnomocněný zástupce uchovává a
zpřístupňuje tuto dokumentaci, včetně prohlášení o shodě,
příslušným orgánům státní správy pro kontrolní účely po dobu
nejméně 5 let po vyrobení posledního zdravotnického
prostředku. Není-li ve státech Evropských společenství
ustanoven výrobce ani jeho zplnomocněný zástupce, udržuje
přístup k technické dokumentaci osoba, která uvádí
zdravotnický prostředek na trh ve státech Evropských
společenství.
3. Technická dokumentace musí umožnit hodnocení shody
zdravotnického prostředku s požadavky tohoto nařízení; tato
dokumentace musí obsahovat zejména náležitosti uvedené
v příloze č. XII bodech 3.1. až 3.5. k tomuto nařízení a dále
3.6. výsledky zejména konstrukčních výpočtů a provedených
kontrol; jestliže ke splnění určeného účelu použití má
být zdravotnický prostředek spojen s jiným zdravotnickým
prostředkem musí být prokázáno, že zdravotnický
prostředek vyhovuje základním požadavkům při spojení s
jiným zdravotnickým prostředkem nebo zdravotnickými
prostředky, který má (které mají) charakteristiky
specifikované výrobcem,
3.7. zkušební zprávy, popřípadě klinické údaje získané podle
zákona o zdravotnických prostředcích,10) popřípadě
přílohy č. XVII k tomuto nařízení,
3.8. označení zdravotnického prostředku ve smyslu § 4 odst. 2
a návod k jeho použití.
4. Výrobce zavede a aktualizuje systematický postup vyhodnocování
informací a zkušeností uživatelů s jím vyrobenými
zdravotnickými prostředky a v návaznosti na uvedenou činnost
provádí odpovídající nápravná opatření, zejména oznamuje vznik
nežádoucích příhod, jakmile se o nich dozví.
5. U zdravotnických prostředků uváděných na trh ve sterilním
stavu a u zdravotnických prostředků třídy I s měřicí funkcí
výrobce dodržuje kromě ustanovení této přílohy i jeden z
postupů podle příloh č. VII, IX nebo XI k tomuto nařízení.
Použití uvedených příloh a opatření autorizované osoby se
omezuje u zdravotnických prostředků
5.1. uváděných na trh ve sterilním stavu pouze na výrobní
hlediska, která se dotýkají zajišťování a udržování
sterilních podmínek,
5.2. s měřicí funkcí pouze na výrobní hlediska, která
souvisejí se shodou těchto prostředků s metrologickými
požadavky,
přičemž lze použít ustanovení bodu 6.1. této přílohy.
6. Použití pro prostředky třídy IIa.
6.1. V souladu s § 9 odst. 2 může být tato příloha použita pro
zdravotnické prostředky třídy IIa s tím, že při jejím
použití ve spojení s postupem podle příloh č. VII, IX
nebo XI k tomuto nařízení tvoří prohlášení o shodě podle
uvedených příloh jediné prohlášení o shodě. V tomto
prohlášení, které vychází z této přílohy, výrobce
zaručuje a prohlašuje, že návrh zdravotnického prostředku
vyhovuje ustanovením, která se na něj vztahují z tohoto
nařízení.
------------------------------------------------------------------
10) § 8 až 16 zákona č. 123/2000 Sb.
Příl.XIV
Prohlášení o zdravotnických prostředcích
pro zvláštní účely
1. Posouzení shody zdravotnických prostředků pro zvláštní účely
je postup, při kterém výrobce nebo dovozce vyhotoví o
zakázkových zdravotnických prostředcích nebo o zdravotnických
prostředcích určených pro klinické zkoušky prohlášení, které
obsahuje údaje uvedené v bodu 2. této přílohy.
2. Prohlášení uvedené v bodu 1. této přílohy musí obsahovat
2.1. u zakázkových zdravotnických prostředků
2.1.1. údaje umožňující identifikaci příslušného
zdravotnického prostředku,
2.1.2. prohlášení, že tento zdravotnický prostředek je
určen výlučně pro určitého pacienta spolu s
uvedením jeho jména a příjmení,
2.1.3. jméno a příjmení lékaře nebo jiné pověřené osoby,
která vypracovala předpis tohoto zdravotnického
prostředku a adresu místa, kde poskytuje
ambulantní nebo ústavní zdravotní péči; u
právnické osoby její název (obchodní firmu),
adresu sídla, kde poskytuje ambulantní nebo
ústavní zdravotní péči,
2.1.4. jednotlivé charakteristiky tohoto zdravotnického
prostředku podle specifikace v příslušném
lékařském předpisu,
2.1.5. prohlášení, že tento zdravotnický prostředek
vyhovuje základním požadavkům, popřípadě údaje,
které z těchto základních požadavků nejsou zcela
splněny včetně odůvodnění.
2.2. u zdravotnických prostředků určených ke klinickým
zkouškám podle zákona o zdravotnických prostředcích10) a
přílohy č. XVII k tomuto nařízení
2.2.1. údaje umožňující identifikaci tohoto prostředku,
2.2.2. plán klinických zkoušek obsahující zejména účel,
vědecké, technické nebo medicínské důvody, rozsah
a počet těchto prostředků zahrnutých do plánu
klinických zkoušek,
2.2.3. stanovisko příslušné etické komise včetně
podrobných údajů souvisejících s tímto
stanoviskem,
2.2.4. jméno a příjmení osoby, která zadává provedení
klinické zkoušky34) a jméno a příjmení lékaře nebo
jiné pověřené osoby, která prakticky provádí
klinickou zkoušku a odpovídá za ně,35)
2.2.5. místo, datum zahájení a plánovaná doba trvání
klinických zkoušek,
2.2.6. prohlášení, že příslušný zdravotnický prostředek
vyhovuje základním požadavkům, s výjimkou
hledisek, které jsou předmětem klinických zkoušek
a že s ohledem na tato hlediska byla učiněna
předběžná opatření k ochraně zdraví a bezpečnosti
pacienta.
3. Výrobce nebo dovozce zpřístupní příslušným úřadům státní
správy
3.1. u zakázkového zdravotnického prostředku dokumentaci
umožňující porozumět návrhu, výrobě a účinnosti (včetně
očekávané účinnosti) tohoto prostředku za účelem
zhodnocení jeho shody s požadavky tohoto nařízení; dále
výrobce učiní nezbytná opatření, aby jeho výrobní proces
produkoval zakázkové zdravotnické prostředky v souladu s
dokumentací uvedenou v části věty před středníkem,
3.2. u zdravotnického prostředku určeného ke klinickým
zkouškám dokumentaci, která musí obsahovat
3.2.1. všeobecný popis tohoto prostředku,
3.2.2. konstrukční výkresy, předpokládané výrobní
technologie, zejména pokud jde o sterilizaci, dále
výkresy částí, podsestav a obvodů,
3.2.3. popisy a vysvětlení nezbytné k porozumění výše
uvedeným výkresům, schématům a činnosti tohoto
prostředku,
3.2.4. výsledky analýzy rizik, seznam částečně nebo plně
použitých norem8) a popis řešení přijatých pro
splnění základních požadavků, jestliže normy8)
nebyly použity,
3.2.5. výsledky konstrukčních výpočtů, provedených
kontrol, technických zkoušek, popřípadě dalších
opatření;
výrobce učiní nezbytná opatření, aby jeho výrobní proces
produkoval zdravotnické prostředky, které odpovídají
dokumentaci podle části věty před středníkem. Výrobce
nebo dovozce zajistí hodnocení účinnosti těchto opatření,
v případě nutnosti pomocí auditu.
4. Výrobce nebo dovozce uchovává pro potřeby příslušných orgánů
státní správy informace obsažené v prohlášeních podle této
přílohy po dobu nejméně 5 let.
------------------------------------------------------------------
8) § 4a odst. 1 zákona č. 22/1997 Sb., o technických požadavcích
na výrobky a o změně a doplnění některých zákonů, ve znění
zákona č. 71/2000 Sb.
10) § 8 až 16 zákona č. 123/2000 Sb.
34) § 13 zákona č. 123/2000 Sb.
35) § 14 zákona č. 123/2000 Sb.
Příl.XV
Prohlášení o zdravotnických prostředcích
pro zvláštní účely
1. Výrobce nebo jeho zplnomocněný zástupce vyhotoví o zakázkových
zdravotnických prostředcích nebo o zdravotnických prostředcích
určených pro klinické zkoušky prohlášení.
2. Prohlášení podle bodu 1. této přílohy musí obsahovat
náležitosti uvedené v bodu 2. přílohy č. XIV k tomuto
nařízení.
3. Výrobce zpřístupňuje příslušným orgánům státní správy
dokumentaci týkající se zakázkových zdravotnických prostředků
a zdravotnických prostředků určených ke klinickým zkouškám
podle přílohy č. XIV bodu 3. k tomuto nařízení; podle téhož
ustanovení výrobce učiní nezbytná opatření, aby jeho výrobní
proces produkoval zdravotnické prostředky, které odpovídají
dokumentaci podle bodů 3.1. a 3.2. přílohy č. XIV k tomuto
nařízení a zajistí hodnocení účinnosti těchto opatření, v
případě nutnosti pomocí auditu.
4. Výrobce nebo jeho zplnomocněný zástupce uchovává pro potřeby
příslušných orgánů státní správy informace obsažené v
prohlášeních podle této přílohy po dobu nejméně 5 let.
Příl.XVI
Klasifikační pravidla
I. Vysvětlivky
1. Seznam vysvětlivek pro klasifikační pravidla:
1.1. trvání
1.1.1. "trvání přechodné" znamená nepřetržité použití
zdravotnického prostředku po dobu kratší než 60
minut,
1.1.2. "trvání krátkodobé" znamená nepřetržité použití
zdravotnického prostředku po dobu kratší než 30
dnů,
1.1.3. "trvání dlouhodobé" znamená nepřetržité použití
zdravotnického prostředku po dobu delší než 30
dnů,
1.2. invazivní prostředky
1.2.1. "tělní otvor" znamená přirozený otvor v těle,
včetně vnějšího povrchu oční bulvy nebo trvalý,
uměle vytvořený otvor,
1.2.2. "invazivní zdravotnický prostředek" znamená
zdravotnický prostředek, který zcela nebo zčásti
proniká do těla tělním otvorem nebo povrchem těla,
1.2.3. "chirurgicky invazivní zdravotnický prostředek"
znamená invazivní zdravotnický prostředek, který
proniká do těla jeho povrchem pomocí chirurgického
zásahu nebo v souvislosti s ním.
Pro účely tohoto nařízení se na zdravotnické
prostředky, které nejsou vymezeny podle předchozí
věty a které pronikají do těla jinak, než
vytvořeným otvorem, pohlíží jako na chirurgické
invazivní zdravotnické prostředky,
1.2.4. "implantabilní zdravotnický prostředek" znamená
zdravotnický prostředek, který má být zcela
zaveden do lidského těla nebo má nahradit
epiteliální povrch nebo povrch oka chirurgickým
zákrokem, po němž má zůstat na místě; za
implantabilní zdravotnický prostředek se rovněž
považuje zdravotnický prostředek, který má být
chirurgickým zákrokem částečně zaveden do lidského
těla a po zákroku v něm zůstat alespoň 30 dní,
1.3. "chirurgický nástroj pro opakované použití" znamená
nástroj určený k chirurgickému řezání, vrtání, řezání
pilkou, škrabání, seškrabávání, svorkování, odtahování,
spínání a podobným postupům, který není spojen s aktivním
zdravotnickým prostředkem a může být po provedení
příslušných postupů znovu použit,
1.4. "aktivní zdravotnický prostředek" znamená zdravotnický
prostředek, jehož činnost závisí na zdroji elektrické
nebo jiné energie, která není přímo vytvářena lidským
tělem nebo gravitací a který působí prostřednictvím
přeměny této energie. Zdravotnické prostředky určené k
přenosu energie nebo látek mezi aktivním zdravotnickým
prostředkem a pacientem bez jakékoliv významné změny se
za aktivní zdravotnický prostředek nepovažují,
1.5. "aktivní terapeutické zařízení" znamená aktivní
zdravotnický prostředek použitý samostatně nebo v
kombinaci s dalšími zdravotnickými prostředky k podpoře,
změně, náhradě, úpravě nebo obnovení biologických funkcí
nebo struktur za účelem léčby nebo zmírnění nemoci,
poranění nebo zdravotního postižení,
1.6. "aktivní diagnostický zdravotnický prostředek" znamená
aktivní zdravotnický prostředek použitý samostatně nebo v
kombinaci s dalšími zdravotnickými prostředky k dodávání
informací pro diagnostikování, monitorování, zjišťování
nebo léčbu fyziologických stavů, stavu zdraví, nemocí
nebo vrozených vad,
1.7. "centrální oběhový systém" znamená pro účely tohoto
nařízení cévy arteriae pulmonales, aorta ascendens,
arteriae coronariae, arteria carotis communis, arteria
carotis externa, arteria carotis interna, arteriae
cerebrales, truncus brachicephalicus, venae cordis, venae
pulmonales, vena cava superior a vena cava inferior,
1.8. "centrální nervový systém" znamená pro účely tohoto
nařízení mozek, mozkové pleny a páteřní míchu.
II. Prováděcí pravidla
2. Prováděcí pravidla.
2.1. Klasifikační pravidla se řídí určeným účelem použití
zdravotnických prostředků.
2.2. Jestliže je zdravotnický prostředek určen k použití v
kombinaci s jiným zdravotnickým prostředkem, uplatní se
klasifikační pravidla pro každý zdravotnický prostředek
samostatně.
Příslušenství se klasifikuje samostatně (odděleně od
zdravotnického prostředku, se kterým se používá).
2.3. Programové vybavení, které řídí nebo ovlivňuje použití
zdravotnického prostředku, patří do stejné třídy jako
tento zdravotnický prostředek.
2.4. Není-li zdravotnický prostředek určen výhradně nebo z
principu k použití pro určitou část těla, posuzuje se a
je klasifikován podle zásady nejkritičtějšího určeného
účelu použití.
2.5. Platí-li pro klasifikaci zdravotnického prostředku
několik pravidel vycházejících z účinnosti tohoto
prostředku a určeného účelu použití, použijí se
nejpřísnější pravidla ve vyšší klasifikační třídě.
III. Klasifikace
Pro klasifikaci druhů zdravotnických prostředků se používají
dále uvedená pravidla v tomto pořadí:
1. Neinvazivní zdravotnické prostředky.
1.1. Pravidlo 1.
Neinvazivní zdravotnické prostředky patří do třídy I,
pokud se na ně nevztahuje některé z dalších pravidel.
1.2. Pravidlo 2.
Neinvazivní zdravotnické prostředky určené pro odvádění
nebo shromažďování krve, tělních tekutin nebo tkání,
tekutin nebo plynů pro případnou infúzi, podávání nebo
zavádění do těla, patří do třídy IIa, jestliže
1.1.2. mohou být připojeny k aktivnímu zdravotnickému
prostředku třídy IIa nebo vyšší třídy,
1.2.2. jsou určeny pro odvádění nebo shromažďování krve
nebo jiných tělních tekutin nebo pro uchovávání
orgánů, částí orgánů nebo tělesných tkání.
Ve všech ostatních případech patří do třídy I.
1.3. Pravidlo 3.
Neinvazivní zdravotnické prostředky určené pro měnění
biologického nebo chemického složení krve, jiných tělních
tekutin nebo jiných tekutin určených pro infúzi do těla
patří do třídy IIb; pokud však léčba spočívá ve filtraci,
odstředění či výměně plynu nebo tepla, patří do třídy
IIa.
1.4. Pravidlo 4.
Neinvazivní zdravotnické prostředky, které přicházejí do
styku s poraněnou kůží patří do
1.4.1. třídy I, jestliže jsou určeny k použití jako
mechanická překážka, ke kompresi nebo k absorpci
výpotků,
1.4.2. třídy IIb, jestliže jsou určeny z principu k
použití u ran, při kterých byla porušena dermis a
mohou mít pouze sekundární terapeutický účinek,
1.4.3. třídy IIa v ostatních případech, včetně
zdravotnických prostředků z principu určených k
ošetření mikroprostředí rány.
2. Invazivní zdravotnické prostředky.
2.1. Pravidlo 5.
Invazivní zdravotnické prostředky, vztahující se k tělním
otvorům, které nejsou chirurgicky invazivními
zdravotnickými prostředky a nejsou určeny k připojení k
aktivnímu zdravotnickému prostředku, patří do
2.1.1. třídy I, jestliže jsou určeny k přechodnému
použití,
2.1.2. třídy IIa, jestliže jsou určeny ke krátkodobému
použití, s výjimkou použití v ústní dutině až po
hltan, ve zvukovodu až po ušní bubínek nebo v
nosní dutině, kdy patří do třídy I,
2.1.3. třídy IIb, jestliže jsou určeny k dlouhodobému
použití, s výjimkou použití v ústní dutině až po
hltan, ve zvukovodu až po ušní bubínek nebo v
nosní dutině a není pravděpodobná jejich absorpce
sliznicí, kdy patří do třídy IIa. Invazivní
zdravotnické prostředky, které se vztahují k
tělním otvorům, a které nejsou chirurgicky
invazivními zdravotnickými prostředky a jsou
určené ke spojení s aktivním zdravotnickým
prostředkem třídy IIa nebo vyšší, patří do třídy
IIa.
2.2. Pravidlo 6.
Chirurgicky invazivní zdravotnické prostředky pro
přechodné použití patří do třídy IIa, jestliže nejsou
2.2.1. specificky určeny pro diagnostikování,
monitorování nebo napravování vad srdce nebo
centrálního oběhového systému přímým stykem s
těmito částmi těla, kdy patří do třídy III,
2.2.2. chirurgickými nástroji pro opakované použití, kdy
patří do třídy I,
2.2.3. určeny k dodávání energie ve formě ionizujícího
záření, kdy patří do třídy IIb,
2.2.4. určeny k vyvolání biologického účinku nebo k
částečné či plné absorpci, kdy patří do třídy IIb,
2.2.5. určeny k podávání léčiv pomocí dávkovacího
systému, postupem z hlediska způsobu aplikace
potenciálně nebezpečným, kdy patří do třídy IIb.
2.3. Pravidlo 7.
Chirurgicky invazivní zdravotnické prostředky pro
krátkodobé použití patří do třídy IIa, jestliže nejsou
určeny
2.3.1. specificky pro diagnostikování, monitorování nebo
napravování vad srdce nebo centrálního oběhového
systému přímým dotykem s těmito částmi těla, kdy
patří do třídy III,
2.3.2. specificky pro použití v přímém dotyku s
centrálním nervovým systémem, kdy patří do třídy
III,
2.3.3. k dodávání energie ve formě ionizujícího záření,
kdy patří do třídy IIb,
2.3.4. k vyvolání biologického účinku nebo k částečné či
plné absorpci, kdy patří do třídy III,
2.3.5. k uskutečnění chemické změny v těle, s výjimkou
zdravotnických prostředků umístěných v zubech,
nebo k podávání léčiv, kdy patří do třídy IIb.
2.4. Pravidlo 8.
Implantabilní a dlouhodobě chirurgicky invazivní
zdravotnické prostředky patří do třídy IIb, jestliže
nejsou určeny k
2.4.1. umístění v zubech, kdy patří do třídy IIa,
2.4.2. použití v přímém dotyku se srdcem, s centrálním
oběhovým nebo centrálním nervovým systémem, kdy
patří do třídy III,
2.4.3. vyvolání biologického účinku nebo k částečné či
plné absorpci, kdy patří do třídy III,
2.4.4. uskutečnění chemické změny v těle s výjimkou
zdravotnických prostředků umístěných v zubech,
nebo k podávání léčiv, kdy patří do třídy III.
3. Dodatečná pravidla pro aktivní zdravotnické prostředky.
3.1. Pravidlo 9.
3.1.1. Aktivní terapeutické zdravotnické prostředky
určené k podávání nebo výměně energie patří do
třídy IIa, jestliže nejsou jejich charakteristiky
takové, že s přihlédnutím k povaze, hustotě a
místu aplikace energie mohou energii do lidského
těla nebo z těla předávat nebo vyměňovat
potenciálně nebezpečným způsobem, kdy patří do
třídy IIb.
3.1.2. Aktivní zdravotnické prostředky určené k řízení
nebo monitorování účinnosti aktivních
terapeutických zdravotnických prostředků třídy IIb
nebo určené přímo k ovlivňování účinnosti takových
zdravotnických prostředků patří do třídy IIb.
3.2. Pravidlo 10.
Aktivní zdravotnické prostředky určené pro diagnostiku
patří do třídy IIa, jestliže jsou určeny k
3.2.1. podávání energie, která je lidským tělem
absorbována, s výjimkou zdravotnických prostředků
používaných k osvětlení pacientova těla ve
viditelném spektru,
3.2.2. zobrazení in vivo distribuce radiofarmak,
3.2.3. přímé diagnostice nebo monitorování životně
důležitých fyziologických procesů, pokud nejsou
specificky určeny k monitorování životně
důležitých fyziologických parametrů, kde povaha
změn je taková, že by mohlo dojít k
bezprostřednímu ohrožení pacienta (například změny
srdečního výkonu, dýchání, činnosti centrální
nervové soustavy), kdy patří do třídy IIb.
Aktivní zdravotnické prostředky určené k emitování
ionizujícího záření a určené pro diagnostickou a terapeutickou
intervenční radiologii, včetně zdravotnických prostředků,
které řídí nebo monitorují takové zdravotnické prostředky či
přímo ovlivňují jejich účinnost, patří do třídy IIb.
3.3. Pravidlo 11.
Aktivní zdravotnické prostředky určené k podávání léčiv,
tělních tekutin nebo jiných látek do těla nebo
odstraňování léčiv, tělních tekutin nebo jiných látek z
těla patří do třídy IIa, pokud se tak nečiní způsobem,
který je potenciálně nebezpečný s přihlédnutím k povaze
používaných látek, částí těla a ke způsobu aplikace, kdy
patří do třídy IIb.
3.4. Pravidlo 12.
Ostatní aktivní zdravotnické prostředky patří do třídy I.
4. Zvláštní pravidla.
4.1. Pravidlo 13.
Zdravotnické prostředky obsahující jako integrální část
látku, která při samostatném použití může být považována
za léčivo a která snadno působí na lidské tělo účinkem
doplňujícím účinek zdravotnického prostředku, patří do
třídy III.
4.2. Pravidlo 14.
Zdravotnické prostředky používané pro antikoncepci nebo k
prevenci přenosu sexuálně přenosných chorob patří do
třídy IIb, jestliže nejsou implantabilními nebo
dlouhodobě invazivními zdravotnickými prostředky, kdy
patří do třídy III.
4.3. Pravidlo 15.
Zdravotnické prostředky specificky určené k použití při
dezinfekci, čištění, oplachování, popřípadě hydrataci
kontaktních čoček, patří do třídy IIb.
Zdravotnické prostředky specificky určené k použití při
dezinfekci zdravotnických prostředků patří do třídy IIa.
Toto pravidlo neplatí pro výrobky určené k fyzickému
čištění zdravotnických prostředků, které nejsou
kontaktními čočkami.
4.4. Pravidlo 16.
Neaktivní zdravotnické prostředky specificky určené pro
záznam diagnostických rentgenových zobrazení patří do
třídy IIa.
4.5. Pravidlo 17.
Zdravotnické prostředky vyrobené s použitím zvířecích
tkání nebo jejich neživých derivátů patří do třídy III, s
výjimkou zdravotnických prostředků, které jsou určeny
pouze ke styku s neporušenou kůží.
5. Pravidlo 18.
Odchylně od jiných pravidel patří krevní vaky do třídy IIb.
Příl.XVII
Bližší podrobnosti klinického hodnocení
1. Obecná ustanovení.
1.1. podmínky, práva a povinnosti osoby, která zadává
provedení klinického hodnocení a klinického výzkumného
pracovníka a dokumentaci klinického hodnocení upravuje
zákon o zdravotnických prostředcích.10)
1.2. Potvrzení shody s požadavky, které se týkají
charakteristik a účinnosti podle přílohy č. I bodu 1.
a 3. k tomuto nařízení za normálních podmínek použití
zdravotnického prostředku a hodnocení nežádoucích
vedlejších účinků, zejména v případě implantabilních
zdravotnických prostředků a zdravotnických prostředků
třídy III, vychází z klinických údajů.
2. Klinické zkoušky musí
2.1. být prováděny v souladu s Helsinskou deklarací přijatou
18. Světovým zdravotnickým shromážděním v roce 1964 v
Helsinkách ve Finsku, změněnou a doplněnou 29. Světovým
lékařským shromážděním v Tokiu v roce 1975, 35. Světovým
lékařským shromážděním v Benátkách v roce 1983 a 41.
Světovým lékařským shromážděním v Hong Kongu v roce 1989,
v Somerset Westu v Jihoafrické republice v roce 1996 a v
Edinburgu v roce 2000 a Úmluvou na ochranu lidských práv
a důstojnosti lidské bytosti v souvislosti s aplikací
biologie a medicíny. Tento požadavek se vztahuje na
klinické zkoušky, a to od první úvahy o jejich potřebě a
oprávněnosti až po zveřejnění výsledků,
2.2. obsahovat odpovídající počet pozorování, aby byla
zaručena vědecká platnost závěrů,
2.3. být provedeny za okolností podobných normálním podmínkám
použití zdravotnického prostředku a
2.4. být vyzkoušeny příslušné charakteristiky zdravotnického
prostředku a jeho vliv na pacienta.
3. Po ukončení klinického hodnocení se zpracovává závěrečná
písemná zpráva; její náležitosti stanoví vyhláška č. 316/2000
Sb., kterou se stanoví náležitosti závěrečné zprávy o
provedeném klinickém hodnocení zdravotnického prostředku.
------------------------------------------------------------------
10) § 8 až 16 zákona č. 123/2000 Sb.
Příl.XVIII
Základní kritéria pro autorizované osoby
Vedle podmínek uvedených ve zvláštním právním předpisu36) Úřad
uděluje autorizaci za předpokladu splnění dalších
následujících podmínek a požadavků:
1. autorizovaná osoba a osoby, které jsou členy jejích
statutárních či jiných orgánů i zaměstnanci autorizované
osoby, kteří jsou zodpovědní za hodnotící a ověřovací činnosti
uvedené v přílohách č. II až XI k tomuto nařízení (dále jen
"hodnocení a ověřování"), nesmějí
1.1. být autorem návrhu zdravotnického prostředku, jeho
výrobcem, distributorem ani osobou provádějící údržbu,
opravy, seřizování a kontroly zdravotnických prostředků
nebo jejich uživatelem těchto prostředků,
1.2. být zplnomocněným zástupcem osoby uvedené v bodu 1,
1.3. podílet se přímo na návrhu, konstrukci, prodeji a
udržování zdravotnických prostředků ani zastupovat strany
zúčastněné na těchto činnostech;
možnost výměny technických informací mezi výrobcem a
autorizovanou osobou není předchozí částí věty dotčena,
2. autorizovaná osoba a její zaměstnanci provádějí hodnocení a
ověřování na soudobé úrovni vědy a techniky, s odpovídající
odborností, zodpovědností, objektivitou a za okolností, které
nemohou ovlivnit jejich úsudek nebo výsledky kontrolní
činnosti, zejména které vylučují vliv osob, majících zájem na
výsledcích hodnocení a ověřování,
3. autorizovaná osoba
3.1. musí být schopná ověřit požadavky vyplývající z přílohy
č. I k tomuto nařízení podle jedné z příloh č. II až XI k
tomuto nařízení a vykonat další úkoly, pro které byla
autorizována nebo může smluvně na svou zodpovědnost
sjednat plnění svých úkolů jinou osobou,
3.2. uchovává pro potřebu příslušných úřadů státní správy
dokumenty o kvalifikaci sjednané osoby a údaje o její
činnosti vykonané podle tohoto nařízení,
3.3. musí mít přístup k materiálnímu a technickému vybavení a
být vybavena zkušenostmi a znalostmi tak, aby mohla řádně
plnit úkoly požadované pro hodnocení a ověřování,
4. zaměstnanci odpovědní za hodnocení a ověřování v rámci
kontrolních postupů musí
4.1. mít odpovídající odbornou praxi pro hodnotící a ověřovací
postupy v rámci obsahu a rozsahu udělené autorizace
autorizované osoby,
4.2. být obeznámena s kontrolní činností, které provádí a
musí mít odpovídající zkušenosti s těmito činnostmi,
4.3. být schopna vypracovat certifikáty nebo ES certifikáty,
záznamy a zprávy prokazující, že kontroly byly provedeny,
4.4. zaručovat nestrannost hodnocení a ověřování,
5. odměny zaměstnanců odpovědných za hodnocení a ověřování
nesmějí být závislé na počtu provedených kontrol ani na jejich
výsledcích,
6. povinnost osob uvedených v návětí v bodu 1. zachovávat
mlčenlivost o skutečnostech, o nichž se dozvídají při činnosti
autorizované osoby stanoví zvláštní právní předpis,37)
7. povinnost autorizované osoby uzavřít smlouvu o pojištění
odpovědnosti za škodu stanoví zvláštní právní předpis.38)
------------------------------------------------------------------
36) § 11 odst. 2 a 3 zákona č. 22/1997 Sb., ve znění zákona č.
71/2000 Sb.
37) § 11 odst. 2 písm. e) zákona č. 22/1997 Sb., ve znění zákona
č. 71/2000 Sb.
38) § 11 odst. 3 zákona č. 22/1997 Sb., ve znění zákona č. 71/2000
Sb.
Příl.XIX
Formulář pro registraci právnických a fyzických osob
Form for Registration of Juristic and Physical Persons
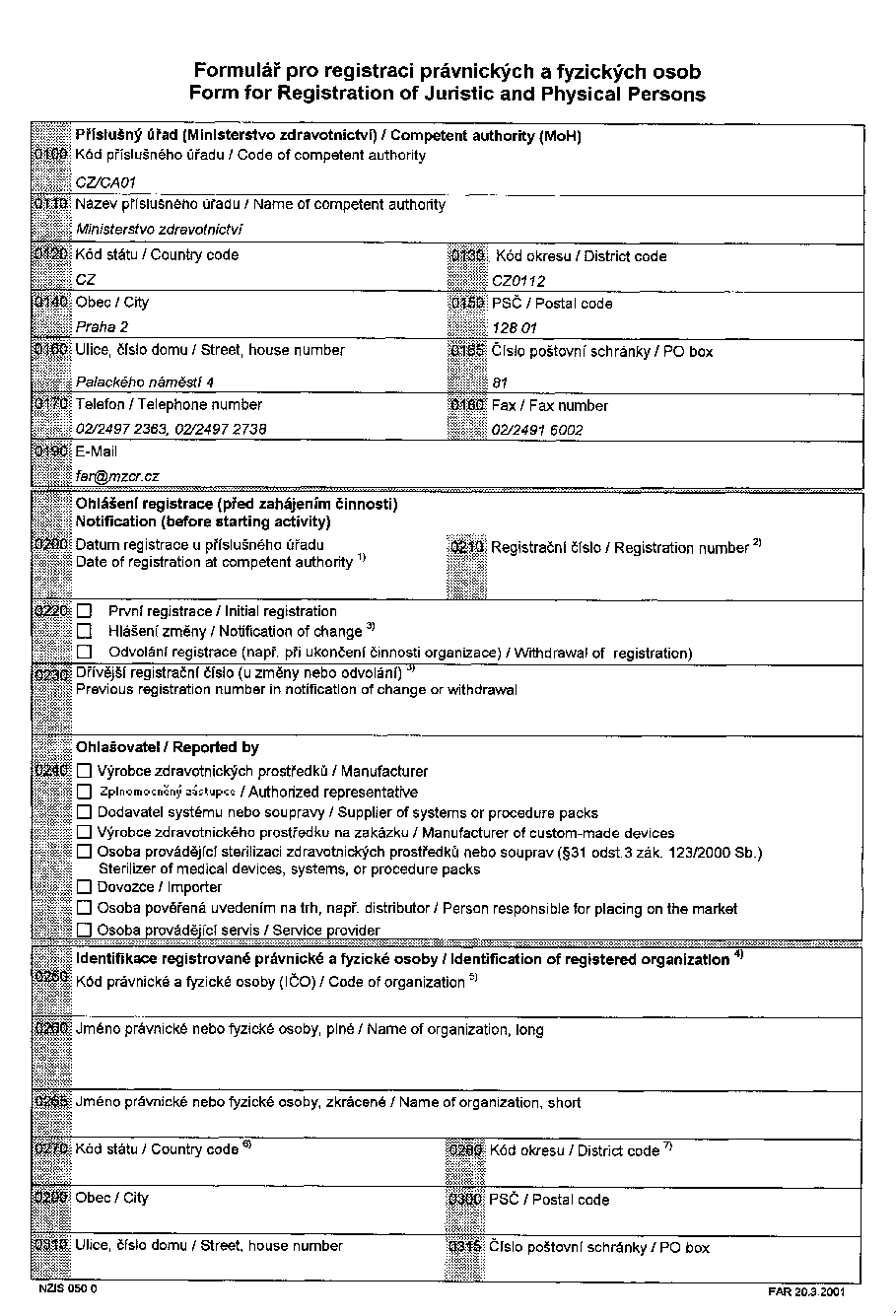
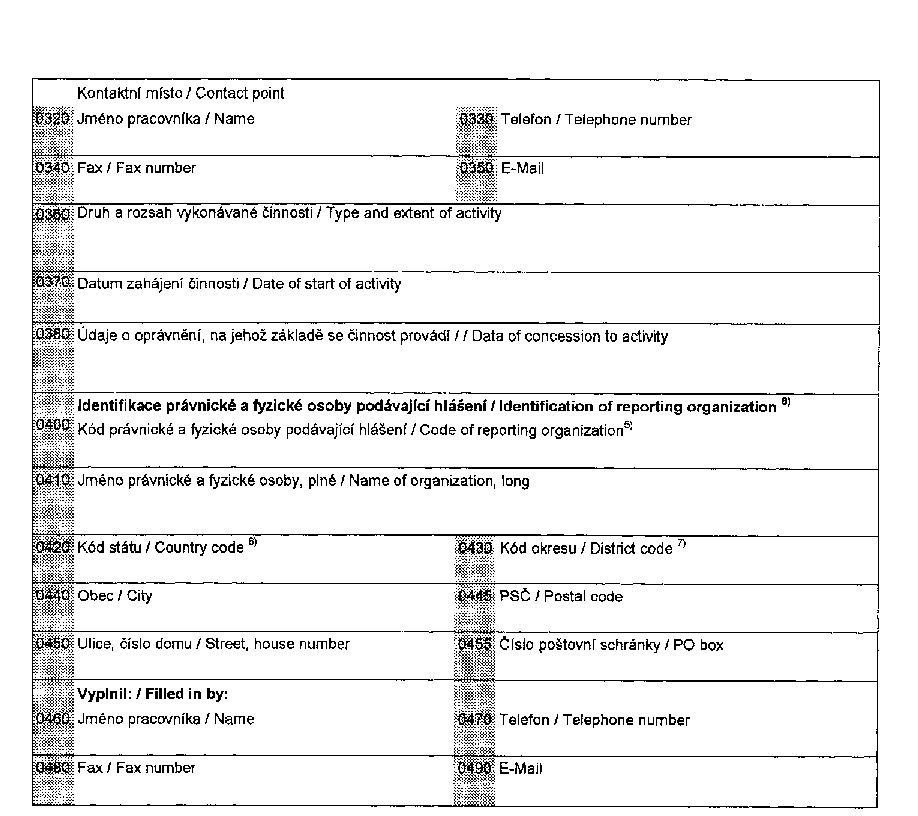 Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí
správné.
I affirm that the information given above is correct to the best
of my knowledge.
Místo ........................ Datum .....................
City Date
Jméno, příjmení ..................... Podpis a razítko...........
Name, long Signature
Poznámky a jiná sdělení:/Notes and other information:9)
Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí
správné.
I affirm that the information given above is correct to the best
of my knowledge.
Místo ........................ Datum .....................
City Date
Jméno, příjmení ..................... Podpis a razítko...........
Name, long Signature
Poznámky a jiná sdělení:/Notes and other information:9)
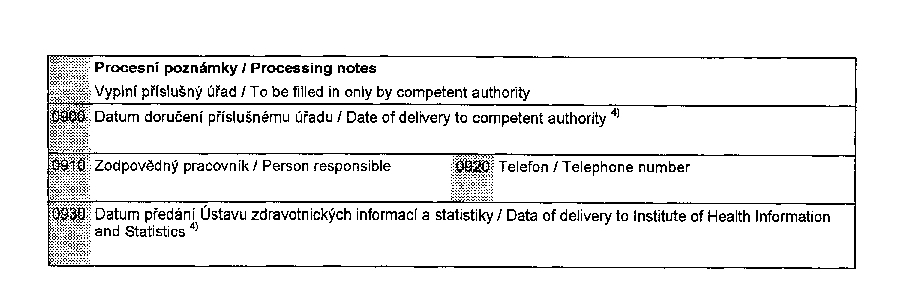 Pokyny k vyplnění formuláře povinné registrace podle § 31 zákona
č. 123/2000 Sb., o zdravotnických prostředcích.
Za každou činnost uvedenou v položce 0240 musí právnické a fyzické
osoby podávající hlášení vyplnit samostatný formulář.
Notes on completing the Obligatory registration form according to
§ 31 Medical Devices Act (No. 123/2000 Coll.)
For each activity stated in item 0240 the notifying organization
must fill in a separate form.
1) Rok, měsíc, den/Year, month, day
2) Bude vydáno příslušným úřadem. Skládá se z dvoumístného kódu
země podle ISO 3166, lomítka, kódu úřadu, lomítka a vnitřního
registračního čísla (nnn..) určeného úřadem: např.:
CZ/CA01/nnn...
2) To be assigned by the competent authority. Composed of the
two-letter country code of ISO 3166 followed by a slash, the
code of the competent authority, a slash and an internal
registration number, e.g.: CZ/CA01/nnn...
3) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení
změny". Mimo změnu položek 0250 (IČO) a 0260 (jméno právnické a
fyzické osoby) lze aktualizovat všechny ostatní. Pokud vznikne
potřeba aktualizace položek 0250 a 0260 je nutno vyplnit novou
registraci ohlašovatele a původní registraci ukončit. Uvádějí
se pouze změněné položky a u položek, které se vypouštějí bez
náhrady se uvede text "vypustit". Při hlášení změny a odvolání
registrace musí být uvedeno "Dřívější registrační číslo".
3) "Notification of change" must be marked for all types of
reported changes. Besides change of item 0250 (VAT-number of
organization) and 0260 (name of organization) all other items
may be updated. If items 0250 or 0260 should be updated it is
necessary to fill in new registration form of organization and
terminate old registration. Only the changed items are filled
in; in items which should be deleted fill in the text
"vypustit". In case change or withdrawal the "Previous
registration number" must be given.
4) Vyplňuje každá fyzická nebo právnická osoba, která má povinnost
registrace podle § 31 odst. 1-3, 5 zákona č. 123/2000 Sb.
4) Is to be filled in by every juristic or physical subject with
obligation to notify according to § 31 Medical Devices Act (No.
123/2000 Coll.).
5) Skládá se z dvoumístného kódu státu (ISO 3166), lomítka a
identifikačního (IČO) čísla výrobce nebo jeho zplnomocněného
zástupce.
5) This code is always composed of the two-letter country code of
ISO 3166 followed by a slash and the identity-number of
manufacturer/representative.
6) Používejte kódy států podle ISO 3166: (1993), např.: Česká
republika CZ.
6) Please use the country codes for the different acc. to ISO 3166
(1993), e.g. for Czech Republic: CZ.
AT ... Rakousko/Austria
BE ... Belgie/Belgium
CH ... Švýcarsko/Switzerland
CZ ... Česká republika/Czech Republic
DE ... Německo/Germany
DK ... Dánsko/Denmark
ES ... Španělsko/Spain
FI ... Finsko/Finland
FR ... Francie/France
GB ... Velká Británie/United Kingdom
GR ... Řecko/Greece
IE ... Irsko/Ireland
IS ... Island/Iceland
IT ... Itálie/Italy
LI ... Lichtenštejnsko/Liechtenstein
LU ... Lucembursko/Luxembourg
NL ... Nizozemí/Netherlands
NO ... Norsko/Norway
PT ... Portugalsko/Portugal
SE ... Švédsko/Sweden
SK ... Slovensko/Slovakia
7) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999,
částka 33/1999 Sb.
7) Please use the district codes prescribed by CSO Disposition
from 27.4.1999, part 33/1999 Coll.
8) Tento oddíl se vyplňuje jen v případě, že registrovaná
právnická a fyzická osoba není totožná s ohlašovatelem, který
registraci hlásí.
8) This part is filled in only if registered organization is
diffrent from reporting subject.
9) Použijte zvláštní list, jestliže je to zapotřebí./Use
additional sheet if necessary.
10) V příloze použijte další listy podle potřeby k soupisu všech
Vámi distribuovaných zdravotnických prostředků, resp.
zdravotnických prostředků, u kterých provádíte servis.
10) Use additional sheet of annex if necessary for the list of all
medical devices supplied or serviced.
Pokyny k vyplnění formuláře povinné registrace podle § 31 zákona
č. 123/2000 Sb., o zdravotnických prostředcích.
Za každou činnost uvedenou v položce 0240 musí právnické a fyzické
osoby podávající hlášení vyplnit samostatný formulář.
Notes on completing the Obligatory registration form according to
§ 31 Medical Devices Act (No. 123/2000 Coll.)
For each activity stated in item 0240 the notifying organization
must fill in a separate form.
1) Rok, měsíc, den/Year, month, day
2) Bude vydáno příslušným úřadem. Skládá se z dvoumístného kódu
země podle ISO 3166, lomítka, kódu úřadu, lomítka a vnitřního
registračního čísla (nnn..) určeného úřadem: např.:
CZ/CA01/nnn...
2) To be assigned by the competent authority. Composed of the
two-letter country code of ISO 3166 followed by a slash, the
code of the competent authority, a slash and an internal
registration number, e.g.: CZ/CA01/nnn...
3) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení
změny". Mimo změnu položek 0250 (IČO) a 0260 (jméno právnické a
fyzické osoby) lze aktualizovat všechny ostatní. Pokud vznikne
potřeba aktualizace položek 0250 a 0260 je nutno vyplnit novou
registraci ohlašovatele a původní registraci ukončit. Uvádějí
se pouze změněné položky a u položek, které se vypouštějí bez
náhrady se uvede text "vypustit". Při hlášení změny a odvolání
registrace musí být uvedeno "Dřívější registrační číslo".
3) "Notification of change" must be marked for all types of
reported changes. Besides change of item 0250 (VAT-number of
organization) and 0260 (name of organization) all other items
may be updated. If items 0250 or 0260 should be updated it is
necessary to fill in new registration form of organization and
terminate old registration. Only the changed items are filled
in; in items which should be deleted fill in the text
"vypustit". In case change or withdrawal the "Previous
registration number" must be given.
4) Vyplňuje každá fyzická nebo právnická osoba, která má povinnost
registrace podle § 31 odst. 1-3, 5 zákona č. 123/2000 Sb.
4) Is to be filled in by every juristic or physical subject with
obligation to notify according to § 31 Medical Devices Act (No.
123/2000 Coll.).
5) Skládá se z dvoumístného kódu státu (ISO 3166), lomítka a
identifikačního (IČO) čísla výrobce nebo jeho zplnomocněného
zástupce.
5) This code is always composed of the two-letter country code of
ISO 3166 followed by a slash and the identity-number of
manufacturer/representative.
6) Používejte kódy států podle ISO 3166: (1993), např.: Česká
republika CZ.
6) Please use the country codes for the different acc. to ISO 3166
(1993), e.g. for Czech Republic: CZ.
AT ... Rakousko/Austria
BE ... Belgie/Belgium
CH ... Švýcarsko/Switzerland
CZ ... Česká republika/Czech Republic
DE ... Německo/Germany
DK ... Dánsko/Denmark
ES ... Španělsko/Spain
FI ... Finsko/Finland
FR ... Francie/France
GB ... Velká Británie/United Kingdom
GR ... Řecko/Greece
IE ... Irsko/Ireland
IS ... Island/Iceland
IT ... Itálie/Italy
LI ... Lichtenštejnsko/Liechtenstein
LU ... Lucembursko/Luxembourg
NL ... Nizozemí/Netherlands
NO ... Norsko/Norway
PT ... Portugalsko/Portugal
SE ... Švédsko/Sweden
SK ... Slovensko/Slovakia
7) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999,
částka 33/1999 Sb.
7) Please use the district codes prescribed by CSO Disposition
from 27.4.1999, part 33/1999 Coll.
8) Tento oddíl se vyplňuje jen v případě, že registrovaná
právnická a fyzická osoba není totožná s ohlašovatelem, který
registraci hlásí.
8) This part is filled in only if registered organization is
diffrent from reporting subject.
9) Použijte zvláštní list, jestliže je to zapotřebí./Use
additional sheet if necessary.
10) V příloze použijte další listy podle potřeby k soupisu všech
Vámi distribuovaných zdravotnických prostředků, resp.
zdravotnických prostředků, u kterých provádíte servis.
10) Use additional sheet of annex if necessary for the list of all
medical devices supplied or serviced.
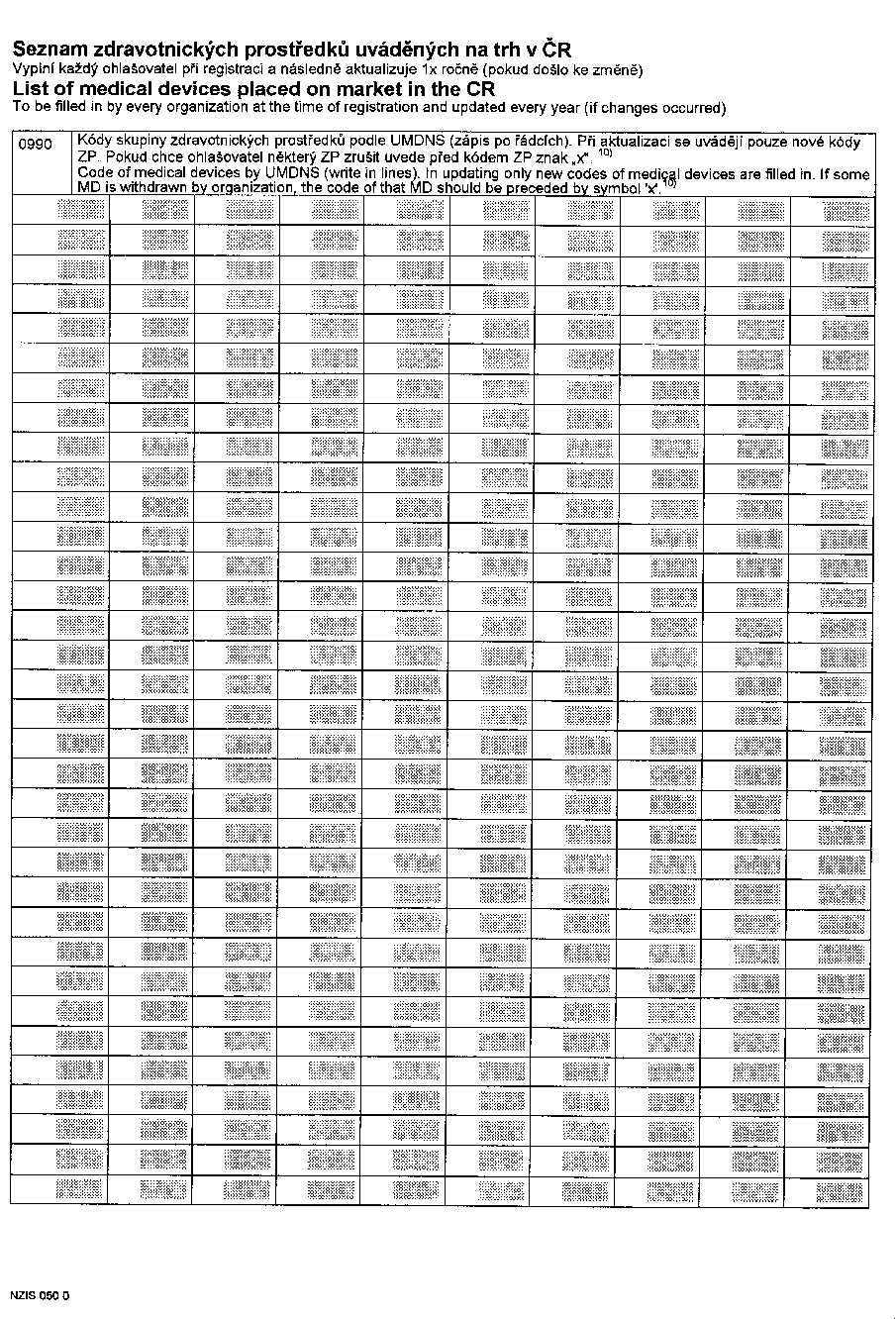 Příl.XX
Formulář pro registraci zdravotnických prostředků
Form for Registration Medical Devices
Příl.XX
Formulář pro registraci zdravotnických prostředků
Form for Registration Medical Devices
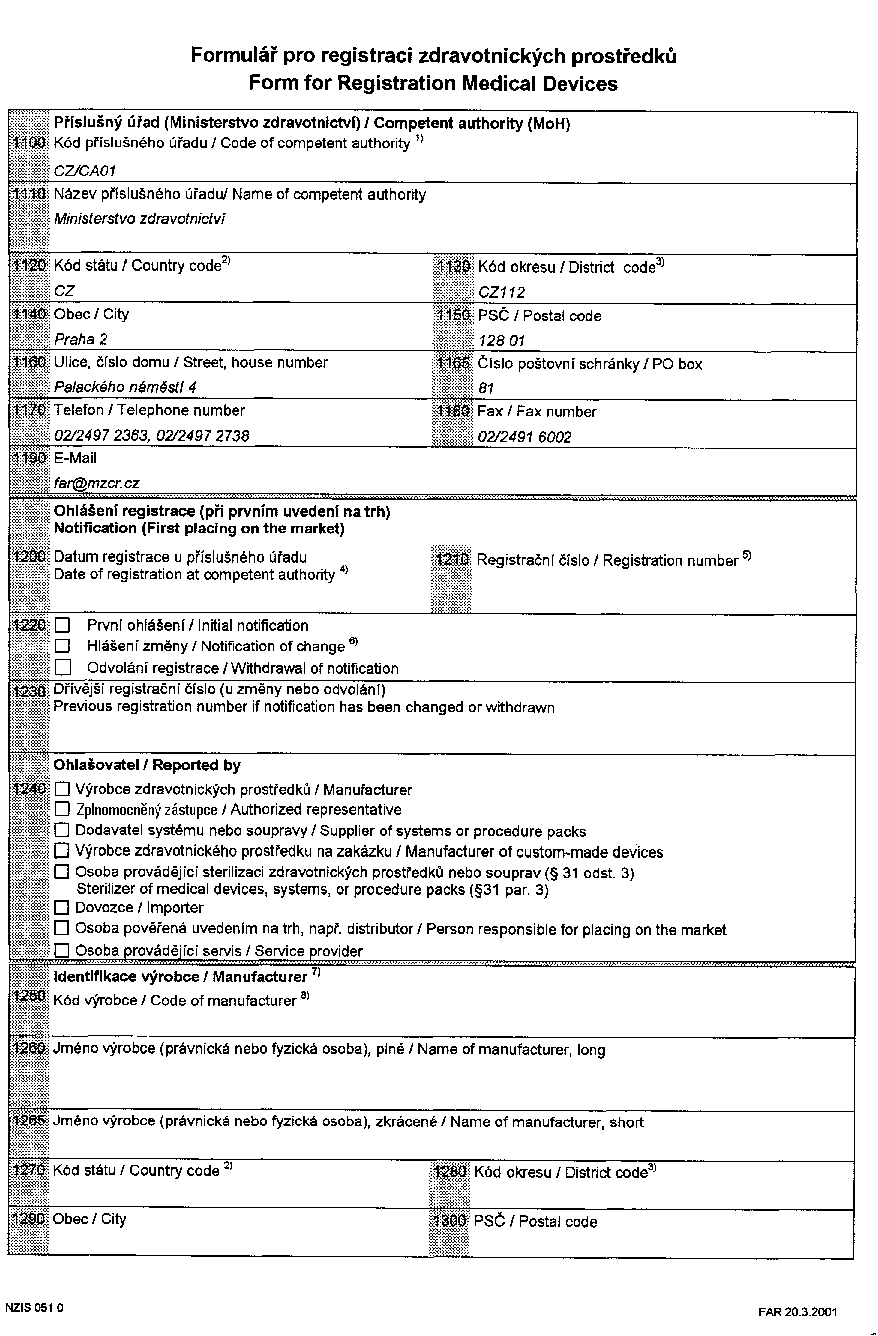
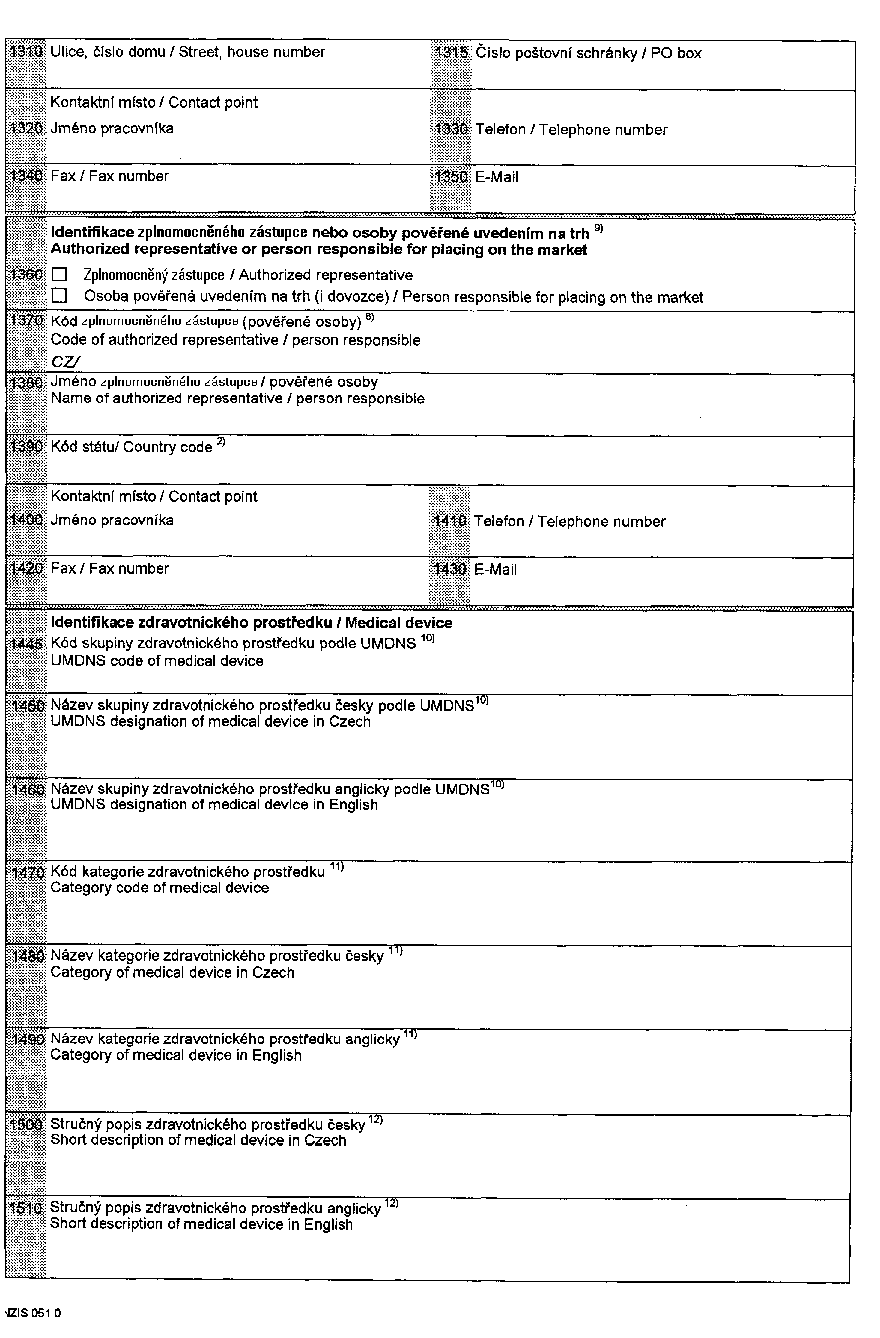
 Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí
správné.
I affirm that the information given above is correct to the best
of my knowledge.
Místo ........................ Datum .....................
City Date
Jméno, příjmení ..................... Podpis a razítko...........
Name, long Signature
Poznámky a jiná sdělení:/Notes and other information:14)
Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí
správné.
I affirm that the information given above is correct to the best
of my knowledge.
Místo ........................ Datum .....................
City Date
Jméno, příjmení ..................... Podpis a razítko...........
Name, long Signature
Poznámky a jiná sdělení:/Notes and other information:14)
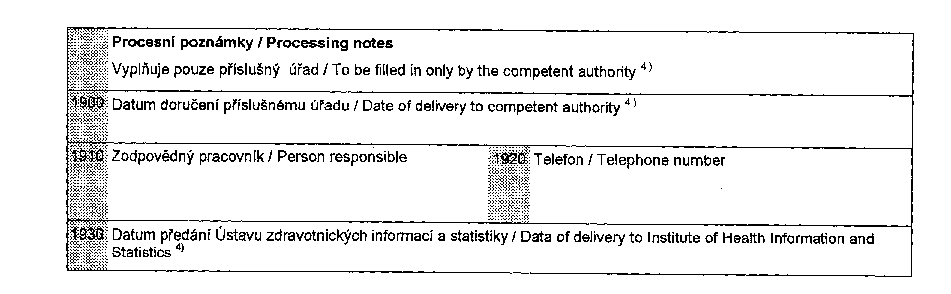 Pokyny k vyplnění formuláře povinného hlášení podle § 31 zákona
č. 123/2000 Sb.
Notes on completing the General Obligation to Notify Form
according to § 31 Medical Devices Act (No. 123/2000 Coll.)
1) Kód příslušného úřadu se skládá z dvoumístného kódu státu podle
ISO 3166, lomítka, písmen CA a čísla příslušného úřadu v daném
státě: například: kód MZ je CZ/CA01.
1) Composed of the two-letter country code of ISO 3166 followed by
a slash, CA and the number of the competent authority in the
state, e.g.: code MoH CR is CZ/CA01.
2) Používejte kódy států podle ISO 3166: (1993), např.:
2) Please use the codes for the different countries acc. to ISO
3166 (1993), e.g.:
AT ... Rakousko/Austria
BE ... Belgie/Belgium
CH ... Švýcarsko/Switzerland
CZ ... Česká republika/Czech Republic
DE ... Německo/Germany
DK ... Dánsko/Denmark
ES ... Španělsko/Spain
FI ... Finsko/Finland
FR ... Francie/France
GB ... Velká Británie/United Kingdom
GR ... Řecko/Greece
IE ... Irsko/Ireland
IS ... Island/Iceland
IT ... Itálie/Italy
LI ... Lichtenštejnsko/Liechtenstein
LU ... Lucembursko/Luxembourg
NL ... Nizozemí/Netherlands
NO ... Norsko/Norway
PT ... Portugalsko/Portugal
SE ... Švédsko/Sweden
SK ... Slovensko/Slovakia
3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999,
částka 33/1999 Sb.
3) Please use the district codes prescribed by CSO Disposition
from 27.4.1999, part 33/1999 Coll.
4) Rok, měsíc, den (v položce 1200 vyplňuje Ministerstvo
zdravotnictví)
4) Year, month, day (column 1200 is filled in by Ministery of
Health)
5) Bude vydáno příslušným úřadem. Skládá se z dvoumístného kódu
státu podle ISO 3166, lomítka a kódu příslušného úřadu, lomítka
a vnitřního registračního čísla určeného úřadem: např.:
CZ/CA01/nnn...
5) To be assigned by the competent authority. Composed of the
two-letter country code of ISO 3166 followed by a slash, the
code of the competent authority, a slash and an internal
registration number, e.g.: CZ/CA01/nnn...
6) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení
změny". Uvádějí se pouze změny, které nemění zařazení
zdravotnických prostředků do klasifikační třídy, do skupiny
zdravotnických prostředků nebo jeho účel použití (tj. položky
1500, 1510, 1580, 1581, 1582). V opačném případě je nutno
provést registraci nového zdravotnického prostředku. Při
"Hlášení změny" nebo "Odvolání změny" musí být uvedeno
"Dřívější registrační číslo". Uvádějí se pouze změněné položky
a u položek, které se vypouštějí bez náhrady se uvede text
"vypustit".
6) In each notificaton of change the box "notification of change"
must be marked. This notification concerns only changes in
which the classification class, group of medical device or the
intended use of the medical device (items 1500, 1510, 1580,
1581, 1582) is not changed. If any of these items is changed,
it is necessary to register a new medical device and terminate
the previous registration. Only the changed items are filled
in; in items which should be deleted fill in the text
"vypustit". For each "Notification of change" or "Withdrawal of
notification" the "previous registration number" must be filled
in.
7) Výroba zahrnuje i montáž, balení, manipulaci, sterilizaci,
obnovu, označování zdravotnického prostředku a určení účelu
jeho použití.
7) Manufacturing also covers e.g. assembling, packaging,
processing, sterilizing, refurbishing, labeling and specifying
the intended purpose of the medical device.
8) Vyplní výrobce nebo jeho zplnomocněný zástupce. Skládá se
z dvoumístného kódu státu (ISO 3166), lomítka a identifikačního
(IČO) čísla výrobce nebo jeho zplnomocněného zástupce.
8) Assigned by the manufacturer or the representative. This code
is always composed of the two-letter country code of ISO 3166
followed by a slash and the identity-number of
manufacturer/representative.
9) Vyplnit jestliže výrobce nemá sídlo v ČR.
9) To be filled in if the manufacturer is not located in the CZ.
10) Uveďte patřičný kód a název skupiny zdravotnického prostředku
podle Univerzálního nomenklaturního systému zdravotnických
prostředků (UMDNS) (např. 10966; obvazy, mul). Není-li
k dispozici, prosím uveďte krátký popis (č. 1500...).
10) Please enter the relevant code and its designation from the
nomenclature Universal Medical Device Nomenclature System
(UMDNS) (e.g. 10966; Compresses, Gauze). If not available,
please give a short description (No. 1500...).
11) Kód a název kategorie jsou založeny na ČSN EN ISO 15225.
Prostředek se označuje kódem první vhodné kategorie, do které
spadá v pořadí od písmene a do písmene l.
11) Device category code and term are based on ČSN EN ISO
15225:2000. The device should be assigned to the first
category in which it fits, moving from a to l.
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|Kód | | |Code| | |
|kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R|
| | | |cat.| | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g|
| |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h|
| |Active implantable devices | | |Electro mechanical medical devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i|
| |Non-active implantable devices | | |opakované použití | |
| | | | |Reusable instruments | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j|
| |Dental devices | | |Single use devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k|
| |prostředky | | |Technical aids for disabled persons | |
| |Ophthalmic and optical devices | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l|
| |a terapii zářením | | |Hospital hardware | |
| |Diagnostic and therapeutic radiation | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
12) Povinné jen pokud nebyl uveden kód a název skupiny
zdravotnického prostředku. Zvolte sami vhodný stručný
(heslovitý) popis. Může obsahovat základní vlastnosti
prostředku, jako např. předpokládané použití, hlavní aspekty
klasifikace, sterilní, metrologické vlastnosti, vztah k
obsaženému léku atd.
12) Only compulsory, if no relevant code/designation has been
given. Please use appropriate terms or a short phrase. It can
include basic features of the product such as, for example,
the intended use, the aspects governing its classification,
sterile, metrological qualities, the relationship to an
incorporated drug, the principal mode of action ...
13) Je možné uvést více položek.
13) Multiple entries possible.
14) Použijte zvláštní list, jestliže je to zapotřebí.
14) Use additional sheet if necessary.
Příl.XXI
Formulář hlášení o klinických zkouškách
Clinical Investigation Notification Form
Pokyny k vyplnění formuláře povinného hlášení podle § 31 zákona
č. 123/2000 Sb.
Notes on completing the General Obligation to Notify Form
according to § 31 Medical Devices Act (No. 123/2000 Coll.)
1) Kód příslušného úřadu se skládá z dvoumístného kódu státu podle
ISO 3166, lomítka, písmen CA a čísla příslušného úřadu v daném
státě: například: kód MZ je CZ/CA01.
1) Composed of the two-letter country code of ISO 3166 followed by
a slash, CA and the number of the competent authority in the
state, e.g.: code MoH CR is CZ/CA01.
2) Používejte kódy států podle ISO 3166: (1993), např.:
2) Please use the codes for the different countries acc. to ISO
3166 (1993), e.g.:
AT ... Rakousko/Austria
BE ... Belgie/Belgium
CH ... Švýcarsko/Switzerland
CZ ... Česká republika/Czech Republic
DE ... Německo/Germany
DK ... Dánsko/Denmark
ES ... Španělsko/Spain
FI ... Finsko/Finland
FR ... Francie/France
GB ... Velká Británie/United Kingdom
GR ... Řecko/Greece
IE ... Irsko/Ireland
IS ... Island/Iceland
IT ... Itálie/Italy
LI ... Lichtenštejnsko/Liechtenstein
LU ... Lucembursko/Luxembourg
NL ... Nizozemí/Netherlands
NO ... Norsko/Norway
PT ... Portugalsko/Portugal
SE ... Švédsko/Sweden
SK ... Slovensko/Slovakia
3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999,
částka 33/1999 Sb.
3) Please use the district codes prescribed by CSO Disposition
from 27.4.1999, part 33/1999 Coll.
4) Rok, měsíc, den (v položce 1200 vyplňuje Ministerstvo
zdravotnictví)
4) Year, month, day (column 1200 is filled in by Ministery of
Health)
5) Bude vydáno příslušným úřadem. Skládá se z dvoumístného kódu
státu podle ISO 3166, lomítka a kódu příslušného úřadu, lomítka
a vnitřního registračního čísla určeného úřadem: např.:
CZ/CA01/nnn...
5) To be assigned by the competent authority. Composed of the
two-letter country code of ISO 3166 followed by a slash, the
code of the competent authority, a slash and an internal
registration number, e.g.: CZ/CA01/nnn...
6) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení
změny". Uvádějí se pouze změny, které nemění zařazení
zdravotnických prostředků do klasifikační třídy, do skupiny
zdravotnických prostředků nebo jeho účel použití (tj. položky
1500, 1510, 1580, 1581, 1582). V opačném případě je nutno
provést registraci nového zdravotnického prostředku. Při
"Hlášení změny" nebo "Odvolání změny" musí být uvedeno
"Dřívější registrační číslo". Uvádějí se pouze změněné položky
a u položek, které se vypouštějí bez náhrady se uvede text
"vypustit".
6) In each notificaton of change the box "notification of change"
must be marked. This notification concerns only changes in
which the classification class, group of medical device or the
intended use of the medical device (items 1500, 1510, 1580,
1581, 1582) is not changed. If any of these items is changed,
it is necessary to register a new medical device and terminate
the previous registration. Only the changed items are filled
in; in items which should be deleted fill in the text
"vypustit". For each "Notification of change" or "Withdrawal of
notification" the "previous registration number" must be filled
in.
7) Výroba zahrnuje i montáž, balení, manipulaci, sterilizaci,
obnovu, označování zdravotnického prostředku a určení účelu
jeho použití.
7) Manufacturing also covers e.g. assembling, packaging,
processing, sterilizing, refurbishing, labeling and specifying
the intended purpose of the medical device.
8) Vyplní výrobce nebo jeho zplnomocněný zástupce. Skládá se
z dvoumístného kódu státu (ISO 3166), lomítka a identifikačního
(IČO) čísla výrobce nebo jeho zplnomocněného zástupce.
8) Assigned by the manufacturer or the representative. This code
is always composed of the two-letter country code of ISO 3166
followed by a slash and the identity-number of
manufacturer/representative.
9) Vyplnit jestliže výrobce nemá sídlo v ČR.
9) To be filled in if the manufacturer is not located in the CZ.
10) Uveďte patřičný kód a název skupiny zdravotnického prostředku
podle Univerzálního nomenklaturního systému zdravotnických
prostředků (UMDNS) (např. 10966; obvazy, mul). Není-li
k dispozici, prosím uveďte krátký popis (č. 1500...).
10) Please enter the relevant code and its designation from the
nomenclature Universal Medical Device Nomenclature System
(UMDNS) (e.g. 10966; Compresses, Gauze). If not available,
please give a short description (No. 1500...).
11) Kód a název kategorie jsou založeny na ČSN EN ISO 15225.
Prostředek se označuje kódem první vhodné kategorie, do které
spadá v pořadí od písmene a do písmene l.
11) Device category code and term are based on ČSN EN ISO
15225:2000. The device should be assigned to the first
category in which it fits, moving from a to l.
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|Kód | | |Code| | |
|kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R|
| | | |cat.| | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g|
| |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h|
| |Active implantable devices | | |Electro mechanical medical devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i|
| |Non-active implantable devices | | |opakované použití | |
| | | | |Reusable instruments | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j|
| |Dental devices | | |Single use devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k|
| |prostředky | | |Technical aids for disabled persons | |
| |Ophthalmic and optical devices | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l|
| |a terapii zářením | | |Hospital hardware | |
| |Diagnostic and therapeutic radiation | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
12) Povinné jen pokud nebyl uveden kód a název skupiny
zdravotnického prostředku. Zvolte sami vhodný stručný
(heslovitý) popis. Může obsahovat základní vlastnosti
prostředku, jako např. předpokládané použití, hlavní aspekty
klasifikace, sterilní, metrologické vlastnosti, vztah k
obsaženému léku atd.
12) Only compulsory, if no relevant code/designation has been
given. Please use appropriate terms or a short phrase. It can
include basic features of the product such as, for example,
the intended use, the aspects governing its classification,
sterile, metrological qualities, the relationship to an
incorporated drug, the principal mode of action ...
13) Je možné uvést více položek.
13) Multiple entries possible.
14) Použijte zvláštní list, jestliže je to zapotřebí.
14) Use additional sheet if necessary.
Příl.XXI
Formulář hlášení o klinických zkouškách
Clinical Investigation Notification Form


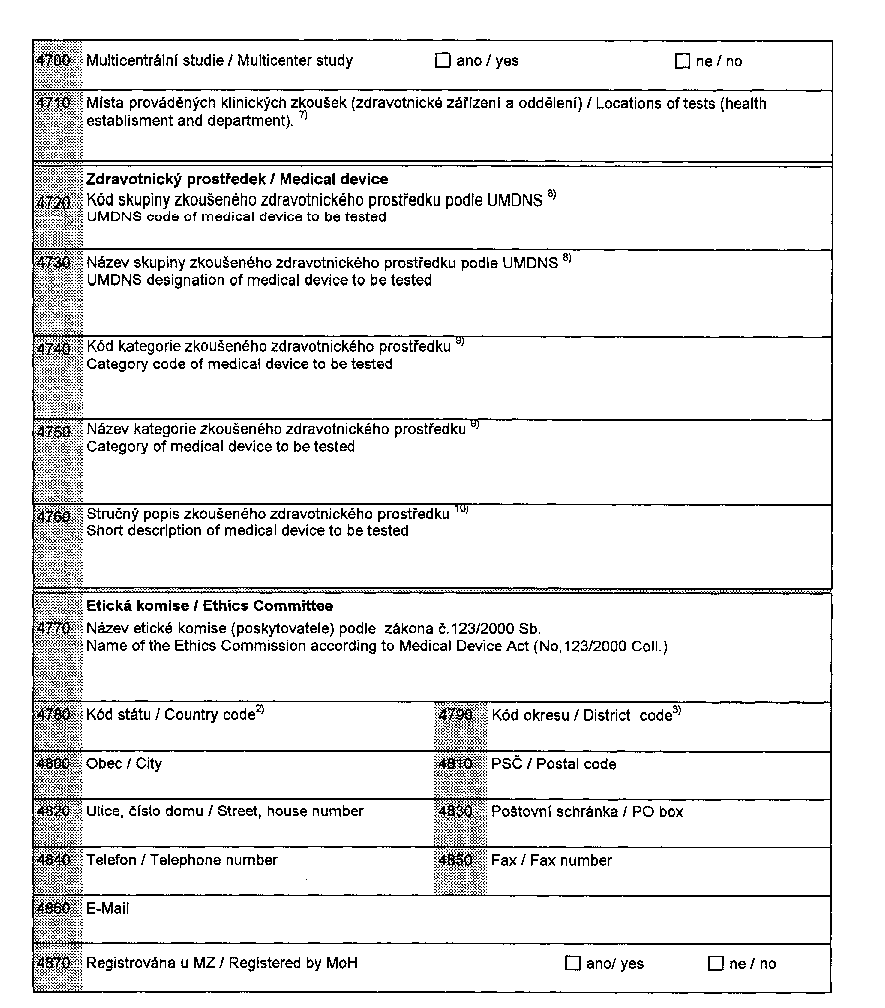
 Obec ........................ Datum .....................
City Date
Jméno, příjmení ..................... Podpis a razítko...........
Name, long Signature
Poznámky a jiná sdělení:/Notes and other information:7)
Obec ........................ Datum .....................
City Date
Jméno, příjmení ..................... Podpis a razítko...........
Name, long Signature
Poznámky a jiná sdělení:/Notes and other information:7)
 Pokyny k vyplnění Formuláře hlášení o klinickém zkoušení podle
zákona č. 123/2000 Sb., o zdravotnických prostředcích a o změně
některých souvisejících zákonů.
Notes on completing the Clinical Investigation Notification Form
according to Medical Devices Act No. 123/2000 Coll.
1) Kód je složen z dvoumístného označení státu podle ISO 3166,
lomítka, písmen CA a čísla příslušného úřadu v daném státě,
např.: kód MZ je CZ/CA01.
1) Composed of the two-letter country code of ISO 3166 followed by
a slash, CA and the number of the competent authority in the
state, e.g.: CZ/CA01.
2) Používejte prosím kódy států podle ISO 3166, např.:
2) Please use the codes for the different countries acc. to ISO
3166 (1993), e.g.:
AT ... Rakousko/Austria
BE ... Belgie/Belgium
CH ... Švýcarsko/Switzerland
CZ ... Česká republika/Czech Republic
DE ... Německo/Germany
DK ... Dánsko/Denmark
ES ... Španělsko/Spain
FI ... Finsko/Finland
FR ... Francie/France
GB ... Velká Británie/United Kingdom
GR ... Řecko/Greece
IE ... Irsko/Ireland
IS ... Island/Iceland
IT ... Itálie/Italy
LI ... Lichtenštejnsko/Liechtenstein
LU ... Lucembursko/Luxembourg
NL ... Nizozemí/Netherlands
NO ... Norsko/Norway
PT ... Portugalsko/Portugal
SE ... Švédsko/Sweden
SK ... Slovensko/Slovakia
3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999,
částka 33/1999 Sb.
3) Please use the district codes prescribed by CSO Disposition
from 27.4.1999, part 33/1999 Coll.
4) Bude vydáno příslušným úřadem. Skládá se z kódu státu podle ISO
3166, lomítka a kódu příslušného úřadu, lomítka a vnitřního
registračního čísla určeného úřadem: např.: CZ/CA01/nnn...
4) To be assigned by the competent authority. Composed of the
two-letter country code of ISO 3166 followed by a slash, the
code of the competent authority, a slash and an internal
registration number, e.g.: CZ/CA01/nnn...
5) Vyplní výrobce nebo zplnomocněný zástupce. Kód je složen
z dvoumístného označení státu podle ISO 3166, lomítka
a identifikačního čísla (IČO) výrobce nebo zplnomocněného
zástupce.
5) Assigned by the manufacturer/authorized representative. This
code is always composed of the two-letter country code of ISO
3166 followed by a slash and the identity-number of
manufacturer/authorized representative.
6) Rok, měsíc, den
6) Year, month, day
7) Použijte další list papíru, jestliže je to třeba. Uveďte
všechna zúčastněná zdravotnická zařízení včetně jejich adresy
(město, stát).
7) Use additional sheet if necessary.
8) Vyplňte správný kód a název skupiny zdravotnického prostředku
podle Univerzálního nomenklaturního systému zdravotnických
prostředků (UMDNS) (např. 16516, kardiostimulátory, vnější
neinvazivní). Pokud není k dispozici, uveďte prosím stručný
popis (číslo kolonky 4760).
8) Please enter the relevant code and its designation from the
nomenclature Universal Medical Device Nomenclature System
(UMDNS) (e.g. 16516; Pacemakers, Cardiac, External
Noninvasive). If not available, please give a short description
(No. 4760).
9) Kód a název kategorie jsou založeny na normě ČSN EN ISO 15225.
Zdravotnický prostředek se označuje kódem první vhodné
kategorie, do které spadá v pořadí od písmene a do písmene l.
9) Device category code and term are based on ČSN EN ISO
15225:2000. The device should be assigned to the first category
in which it fits, moving from a to l.
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|Kód | | |Code| | |
|kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R|
| | | |cat.| | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g|
| |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h|
| |Active implantable devices | | |Electro mechanical medical devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i|
| |Non-active implantable devices | | |opakované použití | |
| | | | |Reusable instruments | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j|
| |Dental devices | | |Single use devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k|
| |prostředky | | |Technical aids for disabled persons | |
| |Ophthalmic and optical devices | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l|
| |a terapii zářením | | |Hospital hardware | |
| |Diagnostic and therapeutic radiation | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
10) Označte důležité informace pro identifikaci zkoušeného
zdravotnického prostředku.
10) Please indicate the necessary data for the identification of
the medical device to be tested.
Příl.XXII
Formulář pro registraci informací vztahujících se
k certifikaci zdravotnických prostředků
Form for the registration of information relating
to the certification of medical devices
Pokyny k vyplnění Formuláře hlášení o klinickém zkoušení podle
zákona č. 123/2000 Sb., o zdravotnických prostředcích a o změně
některých souvisejících zákonů.
Notes on completing the Clinical Investigation Notification Form
according to Medical Devices Act No. 123/2000 Coll.
1) Kód je složen z dvoumístného označení státu podle ISO 3166,
lomítka, písmen CA a čísla příslušného úřadu v daném státě,
např.: kód MZ je CZ/CA01.
1) Composed of the two-letter country code of ISO 3166 followed by
a slash, CA and the number of the competent authority in the
state, e.g.: CZ/CA01.
2) Používejte prosím kódy států podle ISO 3166, např.:
2) Please use the codes for the different countries acc. to ISO
3166 (1993), e.g.:
AT ... Rakousko/Austria
BE ... Belgie/Belgium
CH ... Švýcarsko/Switzerland
CZ ... Česká republika/Czech Republic
DE ... Německo/Germany
DK ... Dánsko/Denmark
ES ... Španělsko/Spain
FI ... Finsko/Finland
FR ... Francie/France
GB ... Velká Británie/United Kingdom
GR ... Řecko/Greece
IE ... Irsko/Ireland
IS ... Island/Iceland
IT ... Itálie/Italy
LI ... Lichtenštejnsko/Liechtenstein
LU ... Lucembursko/Luxembourg
NL ... Nizozemí/Netherlands
NO ... Norsko/Norway
PT ... Portugalsko/Portugal
SE ... Švédsko/Sweden
SK ... Slovensko/Slovakia
3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999,
částka 33/1999 Sb.
3) Please use the district codes prescribed by CSO Disposition
from 27.4.1999, part 33/1999 Coll.
4) Bude vydáno příslušným úřadem. Skládá se z kódu státu podle ISO
3166, lomítka a kódu příslušného úřadu, lomítka a vnitřního
registračního čísla určeného úřadem: např.: CZ/CA01/nnn...
4) To be assigned by the competent authority. Composed of the
two-letter country code of ISO 3166 followed by a slash, the
code of the competent authority, a slash and an internal
registration number, e.g.: CZ/CA01/nnn...
5) Vyplní výrobce nebo zplnomocněný zástupce. Kód je složen
z dvoumístného označení státu podle ISO 3166, lomítka
a identifikačního čísla (IČO) výrobce nebo zplnomocněného
zástupce.
5) Assigned by the manufacturer/authorized representative. This
code is always composed of the two-letter country code of ISO
3166 followed by a slash and the identity-number of
manufacturer/authorized representative.
6) Rok, měsíc, den
6) Year, month, day
7) Použijte další list papíru, jestliže je to třeba. Uveďte
všechna zúčastněná zdravotnická zařízení včetně jejich adresy
(město, stát).
7) Use additional sheet if necessary.
8) Vyplňte správný kód a název skupiny zdravotnického prostředku
podle Univerzálního nomenklaturního systému zdravotnických
prostředků (UMDNS) (např. 16516, kardiostimulátory, vnější
neinvazivní). Pokud není k dispozici, uveďte prosím stručný
popis (číslo kolonky 4760).
8) Please enter the relevant code and its designation from the
nomenclature Universal Medical Device Nomenclature System
(UMDNS) (e.g. 16516; Pacemakers, Cardiac, External
Noninvasive). If not available, please give a short description
(No. 4760).
9) Kód a název kategorie jsou založeny na normě ČSN EN ISO 15225.
Zdravotnický prostředek se označuje kódem první vhodné
kategorie, do které spadá v pořadí od písmene a do písmene l.
9) Device category code and term are based on ČSN EN ISO
15225:2000. The device should be assigned to the first category
in which it fits, moving from a to l.
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|Kód | | |Code| | |
|kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R|
| | | |cat.| | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g|
| |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h|
| |Active implantable devices | | |Electro mechanical medical devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i|
| |Non-active implantable devices | | |opakované použití | |
| | | | |Reusable instruments | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j|
| |Dental devices | | |Single use devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k|
| |prostředky | | |Technical aids for disabled persons | |
| |Ophthalmic and optical devices | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l|
| |a terapii zářením | | |Hospital hardware | |
| |Diagnostic and therapeutic radiation | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
10) Označte důležité informace pro identifikaci zkoušeného
zdravotnického prostředku.
10) Please indicate the necessary data for the identification of
the medical device to be tested.
Příl.XXII
Formulář pro registraci informací vztahujících se
k certifikaci zdravotnických prostředků
Form for the registration of information relating
to the certification of medical devices



 Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí
správné.
I affirm that the information given above is correct to the best
of my knowledge.
Obec ........................ Datum .....................
City Date
Jméno, příjmení ..................... Podpis a razítko...........
Name, long Signature
Poznámky a jiná sdělení:/Notes and other information:10)
Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí
správné.
I affirm that the information given above is correct to the best
of my knowledge.
Obec ........................ Datum .....................
City Date
Jméno, příjmení ..................... Podpis a razítko...........
Name, long Signature
Poznámky a jiná sdělení:/Notes and other information:10)
 Pokyny k vyplnění formuláře povinného hlášení podle § 31 zákona č.
123/2000 Sb.
Notes on completing the General Obligation to Notify Form
according to § 31 Medical Devices Act No. 123/2000 Coll.
1) Kód příslušného úřadu se skládá z dvoumístného kódu státu podle
ISO 3166, lomítka, písmen CA a čísla příslušného úřadu v daném
státě, například: kód MZ je CZ/CA01.
1) Composed of the two-letter country code of ISO 3166 followed by
a slash, CA and the number of the competent authority in the
state, e.g.: code MoH CR is CZ/CA01.
2) Používejte kódy států podle ISO 3166:
2) Please use the codes for the different countries acc. to ISO
3166 (1993), e.g.:
AT ... Rakousko/Austria
BE ... Belgie/Belgium
CH ... Švýcarsko/Switzerland
CZ ... Česká republika/Czech Republic
DE ... Německo/Germany
DK ... Dánsko/Denmark
ES ... Španělsko/Spain
FI ... Finsko/Finland
FR ... Francie/France
GB ... Velká Británie/United Kingdom
GR ... Řecko/Greece
IE ... Irsko/Ireland
IS ... Island/Iceland
IT ... Itálie/Italy
LI ... Lichtenštejnsko/Liechtenstein
LU ... Lucembursko/Luxembourg
NL ... Nizozemí/Netherlands
NO ... Norsko/Norway
PT ... Portugalsko/Portugal
SE ... Švédsko/Sweden
SK ... Slovensko/Slovakia
3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999,
částka 33/1999 Sb.
3) Please use the district codes prescribed by CSO Disposition
from 27.4.1999, part 33/1999 Coll.
4) Rok, měsíc, den
4) Year, month, day
5) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení
změny". Uvádějí se pouze změny, které nemění zařazení
zdravotnických prostředků do klasifikační třídy, do skupiny
zdravotnické prostředky nebo jeho určený účel použití tj.
položky 5320, 5620, 5630). V opačném případě je nutno provést
registraci nového zdravotnického prostředku. Uvádějí se pouze
změněné položky a u položek, které se vypouštějí bez náhrady se
uvede text "vypustit". Při "Hlášení změny" musí být uvedeno
"Dřívější registrační číslo".
5) In each notificaton of change the box "notification of change"
must be marked. This notification concerns only changes in
which the classification class, group of medical device or the
intended use of the medical device (items 5320, 5620, 5630) is
not changed. If any of these items is changed, it is necessary
to register a new medical device and terminate the previous
registration. Only the changed items are filled in; in items
which should be deleted fill in the text "vypustit". Each
"Notification of change" the "previous registration number"
must be filled in.
6) Vydání, odvolání, pozastavení, odmítnutí a ukončení se vztahují
k certifikátu; změny a doplnění se vztahují k certifikaci
zdravotnického prostředku. Seznam zdravotnických prostředků je
možno rozšířit nebo modifikovat v rozsahu certifikátu systému
úplného zabezpečení jakosti.
6) Issued, withdrawn, suspended, refused and terminated is
certificate-related. Modified and complemented is
product-related. Under a given certificate for a full quality
assurance system, the list of products can be enlarged
(complemented) or products may be modified.
7) Toto číslo je vydáno příslušnou autorizovanou osobou.
7) This number is issued by the Notified Body involved.
8) Certifikát má být vydán autorizovanou osobou pro každou
schválenou šarži (resp. pro každý jednotlivý zdravotnický
prostředek). Pro informaci poskytovanou v rámci výměny dat mezi
výrobcem a autorizovanou osobou postačuje najít v databázi druh
certifikátu vydaného výrobci pro daný zdravotnický prostředek a
identifikovat (kódem) autorizované osoby, která jej vydala.
8) For EC verification, the directives require the Notified Bodies
to issue a certificate for each batch (or for each individual
product) which is accepted. For the information provided in the
context of the regulatory data exchange by a given Notified
Body, it is sufficient to find in the data base the kind of
certificate which has been granted to the manufactuer of a
given device and the identity of the Notified Body which issued
it.
9) To se vztahuje i k orgánům posuzujícím shodu v souladu s
dohodami o vzájemném uznávání certifikace mezi EU a dalšími
státy.
9) This also applies accordingly to conformity assessment bodies
designated in the Mutual Recognition Agreements.
10) V případě potřeby použijte další listy.
10) Use additional sheet if necessary.
11) Vyplní výrobce nebo zplnomocněný zástupce. Skládá se
z dvoumístného kódu státu podle ISO 3166, lomítka
a identifikačního (IČO) čísla výrobce nebo zplnomocněného
zástupce.
11) Assigned by the manufacturer or the representative. This code
is always composed of the two-letter country code of ISO 3166
followed by a slash and the identity-number of
manufacturer/representative.
12) Vyplnit pokud výrobce není v ČR.
12) To be filled in if the manufacturer is not located in the CZ.
13) Určitý výrobní model nebo varianta modelu podle specifikace
uvedené v certifikátu. Údaj povinný pro certifikáty podle bodu
4 přílohy II nebo podle přílohy III nebo podle přílohy IV,
nepovinný pro ostatní certifikáty.
13) Specific manufacturer model or family model as specified in
the certificate. Mandatory for a certificate issued against
point 4 of annex 2/II or against annex 3/III or against annex
4/IV; optional for other certificates.
14) Uvádějte označení a kód podle Univerzálního nomenklaturního
systému zdravotnických prostředků (UMDNS). Pozor: Udejte jen
jedno označení pro jeden zdravotnický prostředek (např. 16516
stimulátory, srdeční, vnější neinvasivní). Pokud není k
dispozici, udejte prosím stručný popis (č. 5620...). Pro každý
další zdravotnický prostředek použijte zvláštní kopii této
stránky.
14) Generic device group code and term have to be taken from ECRI
Universal Medical Device Nomenclature System (UMDNS). Please
note: Only one generic device code/term should be taken for
one medical device (e.g. 16516; Pacemakers, Cardiac, External
Noninvasive). If not available, please give a short
description (No. 5620...). Please use for each additional
medical device a separate copy of this page.
15) Kód a název kategorie jsou založeny na normě ČSN EN ISO 15225.
Výrobek se označuje kódem první vhodné kategorie, do které
spadá v pořadí od písmene a do písmene l.
15) Device category code and term are based on CSN EN ISO
15225:2000. The device should be assigned to the first
category in which it fits, moving from a to l.
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|Kód | | |Code| | |
|kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R|
| | | |cat.| | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g|
| |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h|
| |Active implantable devices | | |Electro mechanical medical devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i|
| |Non-active implantable devices | | |opakované použití | |
| | | | |Reusable instruments | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j|
| |Dental devices | | |Single use devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k|
| |prostředky | | |Technical aids for disabled persons | |
| |Ophthalmic and optical devices | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l|
| |a terapii zářením | | |Hospital hardware | |
| |Diagnostic and therapeutic radiation | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
16) Povinné jen v případě, že nebylo udáno označení a kód. Uveďte
vlastní označení nebo stručnou větu. Ta může zahrnovat hlavní
rysy zdravotnického prostředku, např. předpokládané použití,
významné aspekty pro jeho klasifikaci, sterilní nebo měřicí
vlastnosti, vztah k obsaženým léčivům ...
16) Only compulsory, if no relevant code/designation has been
given. Please use appropriate terms or a short phrase. The
phrase can include basic features of the product such as, for
example, the intended use, the aspects governing its
classification, the sterile or metrological qualitfication,
the relationship with an incorporated drug, the principal
means of action ...
Pokyny k vyplnění formuláře povinného hlášení podle § 31 zákona č.
123/2000 Sb.
Notes on completing the General Obligation to Notify Form
according to § 31 Medical Devices Act No. 123/2000 Coll.
1) Kód příslušného úřadu se skládá z dvoumístného kódu státu podle
ISO 3166, lomítka, písmen CA a čísla příslušného úřadu v daném
státě, například: kód MZ je CZ/CA01.
1) Composed of the two-letter country code of ISO 3166 followed by
a slash, CA and the number of the competent authority in the
state, e.g.: code MoH CR is CZ/CA01.
2) Používejte kódy států podle ISO 3166:
2) Please use the codes for the different countries acc. to ISO
3166 (1993), e.g.:
AT ... Rakousko/Austria
BE ... Belgie/Belgium
CH ... Švýcarsko/Switzerland
CZ ... Česká republika/Czech Republic
DE ... Německo/Germany
DK ... Dánsko/Denmark
ES ... Španělsko/Spain
FI ... Finsko/Finland
FR ... Francie/France
GB ... Velká Británie/United Kingdom
GR ... Řecko/Greece
IE ... Irsko/Ireland
IS ... Island/Iceland
IT ... Itálie/Italy
LI ... Lichtenštejnsko/Liechtenstein
LU ... Lucembursko/Luxembourg
NL ... Nizozemí/Netherlands
NO ... Norsko/Norway
PT ... Portugalsko/Portugal
SE ... Švédsko/Sweden
SK ... Slovensko/Slovakia
3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999,
částka 33/1999 Sb.
3) Please use the district codes prescribed by CSO Disposition
from 27.4.1999, part 33/1999 Coll.
4) Rok, měsíc, den
4) Year, month, day
5) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení
změny". Uvádějí se pouze změny, které nemění zařazení
zdravotnických prostředků do klasifikační třídy, do skupiny
zdravotnické prostředky nebo jeho určený účel použití tj.
položky 5320, 5620, 5630). V opačném případě je nutno provést
registraci nového zdravotnického prostředku. Uvádějí se pouze
změněné položky a u položek, které se vypouštějí bez náhrady se
uvede text "vypustit". Při "Hlášení změny" musí být uvedeno
"Dřívější registrační číslo".
5) In each notificaton of change the box "notification of change"
must be marked. This notification concerns only changes in
which the classification class, group of medical device or the
intended use of the medical device (items 5320, 5620, 5630) is
not changed. If any of these items is changed, it is necessary
to register a new medical device and terminate the previous
registration. Only the changed items are filled in; in items
which should be deleted fill in the text "vypustit". Each
"Notification of change" the "previous registration number"
must be filled in.
6) Vydání, odvolání, pozastavení, odmítnutí a ukončení se vztahují
k certifikátu; změny a doplnění se vztahují k certifikaci
zdravotnického prostředku. Seznam zdravotnických prostředků je
možno rozšířit nebo modifikovat v rozsahu certifikátu systému
úplného zabezpečení jakosti.
6) Issued, withdrawn, suspended, refused and terminated is
certificate-related. Modified and complemented is
product-related. Under a given certificate for a full quality
assurance system, the list of products can be enlarged
(complemented) or products may be modified.
7) Toto číslo je vydáno příslušnou autorizovanou osobou.
7) This number is issued by the Notified Body involved.
8) Certifikát má být vydán autorizovanou osobou pro každou
schválenou šarži (resp. pro každý jednotlivý zdravotnický
prostředek). Pro informaci poskytovanou v rámci výměny dat mezi
výrobcem a autorizovanou osobou postačuje najít v databázi druh
certifikátu vydaného výrobci pro daný zdravotnický prostředek a
identifikovat (kódem) autorizované osoby, která jej vydala.
8) For EC verification, the directives require the Notified Bodies
to issue a certificate for each batch (or for each individual
product) which is accepted. For the information provided in the
context of the regulatory data exchange by a given Notified
Body, it is sufficient to find in the data base the kind of
certificate which has been granted to the manufactuer of a
given device and the identity of the Notified Body which issued
it.
9) To se vztahuje i k orgánům posuzujícím shodu v souladu s
dohodami o vzájemném uznávání certifikace mezi EU a dalšími
státy.
9) This also applies accordingly to conformity assessment bodies
designated in the Mutual Recognition Agreements.
10) V případě potřeby použijte další listy.
10) Use additional sheet if necessary.
11) Vyplní výrobce nebo zplnomocněný zástupce. Skládá se
z dvoumístného kódu státu podle ISO 3166, lomítka
a identifikačního (IČO) čísla výrobce nebo zplnomocněného
zástupce.
11) Assigned by the manufacturer or the representative. This code
is always composed of the two-letter country code of ISO 3166
followed by a slash and the identity-number of
manufacturer/representative.
12) Vyplnit pokud výrobce není v ČR.
12) To be filled in if the manufacturer is not located in the CZ.
13) Určitý výrobní model nebo varianta modelu podle specifikace
uvedené v certifikátu. Údaj povinný pro certifikáty podle bodu
4 přílohy II nebo podle přílohy III nebo podle přílohy IV,
nepovinný pro ostatní certifikáty.
13) Specific manufacturer model or family model as specified in
the certificate. Mandatory for a certificate issued against
point 4 of annex 2/II or against annex 3/III or against annex
4/IV; optional for other certificates.
14) Uvádějte označení a kód podle Univerzálního nomenklaturního
systému zdravotnických prostředků (UMDNS). Pozor: Udejte jen
jedno označení pro jeden zdravotnický prostředek (např. 16516
stimulátory, srdeční, vnější neinvasivní). Pokud není k
dispozici, udejte prosím stručný popis (č. 5620...). Pro každý
další zdravotnický prostředek použijte zvláštní kopii této
stránky.
14) Generic device group code and term have to be taken from ECRI
Universal Medical Device Nomenclature System (UMDNS). Please
note: Only one generic device code/term should be taken for
one medical device (e.g. 16516; Pacemakers, Cardiac, External
Noninvasive). If not available, please give a short
description (No. 5620...). Please use for each additional
medical device a separate copy of this page.
15) Kód a název kategorie jsou založeny na normě ČSN EN ISO 15225.
Výrobek se označuje kódem první vhodné kategorie, do které
spadá v pořadí od písmene a do písmene l.
15) Device category code and term are based on CSN EN ISO
15225:2000. The device should be assigned to the first
category in which it fits, moving from a to l.
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|Kód | | |Code| | |
|kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R|
| | | |cat.| | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g|
| |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h|
| |Active implantable devices | | |Electro mechanical medical devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i|
| |Non-active implantable devices | | |opakované použití | |
| | | | |Reusable instruments | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j|
| |Dental devices | | |Single use devices | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k|
| |prostředky | | |Technical aids for disabled persons | |
| |Ophthalmic and optical devices | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
|12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l|
| |a terapii zářením | | |Hospital hardware | |
| |Diagnostic and therapeutic radiation | | | | |
+----+-----------------------------------------------+-+----+------------------------------------------------+-+
16) Povinné jen v případě, že nebylo udáno označení a kód. Uveďte
vlastní označení nebo stručnou větu. Ta může zahrnovat hlavní
rysy zdravotnického prostředku, např. předpokládané použití,
významné aspekty pro jeho klasifikaci, sterilní nebo měřicí
vlastnosti, vztah k obsaženým léčivům ...
16) Only compulsory, if no relevant code/designation has been
given. Please use appropriate terms or a short phrase. The
phrase can include basic features of the product such as, for
example, the intended use, the aspects governing its
classification, the sterile or metrological qualitfication,
the relationship with an incorporated drug, the principal
means of action ...

Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí správné. I affirm that the information given above is correct to the best of my knowledge. Místo ........................ Datum ..................... City Date Jméno, příjmení ..................... Podpis a razítko........... Name, long Signature Poznámky a jiná sdělení:/Notes and other information:9)
Pokyny k vyplnění formuláře povinné registrace podle § 31 zákona č. 123/2000 Sb., o zdravotnických prostředcích. Za každou činnost uvedenou v položce 0240 musí právnické a fyzické osoby podávající hlášení vyplnit samostatný formulář. Notes on completing the Obligatory registration form according to § 31 Medical Devices Act (No. 123/2000 Coll.) For each activity stated in item 0240 the notifying organization must fill in a separate form. 1) Rok, měsíc, den/Year, month, day 2) Bude vydáno příslušným úřadem. Skládá se z dvoumístného kódu země podle ISO 3166, lomítka, kódu úřadu, lomítka a vnitřního registračního čísla (nnn..) určeného úřadem: např.: CZ/CA01/nnn... 2) To be assigned by the competent authority. Composed of the two-letter country code of ISO 3166 followed by a slash, the code of the competent authority, a slash and an internal registration number, e.g.: CZ/CA01/nnn... 3) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení změny". Mimo změnu položek 0250 (IČO) a 0260 (jméno právnické a fyzické osoby) lze aktualizovat všechny ostatní. Pokud vznikne potřeba aktualizace položek 0250 a 0260 je nutno vyplnit novou registraci ohlašovatele a původní registraci ukončit. Uvádějí se pouze změněné položky a u položek, které se vypouštějí bez náhrady se uvede text "vypustit". Při hlášení změny a odvolání registrace musí být uvedeno "Dřívější registrační číslo". 3) "Notification of change" must be marked for all types of reported changes. Besides change of item 0250 (VAT-number of organization) and 0260 (name of organization) all other items may be updated. If items 0250 or 0260 should be updated it is necessary to fill in new registration form of organization and terminate old registration. Only the changed items are filled in; in items which should be deleted fill in the text "vypustit". In case change or withdrawal the "Previous registration number" must be given. 4) Vyplňuje každá fyzická nebo právnická osoba, která má povinnost registrace podle § 31 odst. 1-3, 5 zákona č. 123/2000 Sb. 4) Is to be filled in by every juristic or physical subject with obligation to notify according to § 31 Medical Devices Act (No. 123/2000 Coll.). 5) Skládá se z dvoumístného kódu státu (ISO 3166), lomítka a identifikačního (IČO) čísla výrobce nebo jeho zplnomocněného zástupce. 5) This code is always composed of the two-letter country code of ISO 3166 followed by a slash and the identity-number of manufacturer/representative. 6) Používejte kódy států podle ISO 3166: (1993), např.: Česká republika CZ. 6) Please use the country codes for the different acc. to ISO 3166 (1993), e.g. for Czech Republic: CZ. AT ... Rakousko/Austria BE ... Belgie/Belgium CH ... Švýcarsko/Switzerland CZ ... Česká republika/Czech Republic DE ... Německo/Germany DK ... Dánsko/Denmark ES ... Španělsko/Spain FI ... Finsko/Finland FR ... Francie/France GB ... Velká Británie/United Kingdom GR ... Řecko/Greece IE ... Irsko/Ireland IS ... Island/Iceland IT ... Itálie/Italy LI ... Lichtenštejnsko/Liechtenstein LU ... Lucembursko/Luxembourg NL ... Nizozemí/Netherlands NO ... Norsko/Norway PT ... Portugalsko/Portugal SE ... Švédsko/Sweden SK ... Slovensko/Slovakia 7) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999, částka 33/1999 Sb. 7) Please use the district codes prescribed by CSO Disposition from 27.4.1999, part 33/1999 Coll. 8) Tento oddíl se vyplňuje jen v případě, že registrovaná právnická a fyzická osoba není totožná s ohlašovatelem, který registraci hlásí. 8) This part is filled in only if registered organization is diffrent from reporting subject. 9) Použijte zvláštní list, jestliže je to zapotřebí./Use additional sheet if necessary. 10) V příloze použijte další listy podle potřeby k soupisu všech Vámi distribuovaných zdravotnických prostředků, resp. zdravotnických prostředků, u kterých provádíte servis. 10) Use additional sheet of annex if necessary for the list of all medical devices supplied or serviced.
Příl.XX Formulář pro registraci zdravotnických prostředků Form for Registration Medical Devices


Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí správné. I affirm that the information given above is correct to the best of my knowledge. Místo ........................ Datum ..................... City Date Jméno, příjmení ..................... Podpis a razítko........... Name, long Signature Poznámky a jiná sdělení:/Notes and other information:14)
Pokyny k vyplnění formuláře povinného hlášení podle § 31 zákona č. 123/2000 Sb. Notes on completing the General Obligation to Notify Form according to § 31 Medical Devices Act (No. 123/2000 Coll.) 1) Kód příslušného úřadu se skládá z dvoumístného kódu státu podle ISO 3166, lomítka, písmen CA a čísla příslušného úřadu v daném státě: například: kód MZ je CZ/CA01. 1) Composed of the two-letter country code of ISO 3166 followed by a slash, CA and the number of the competent authority in the state, e.g.: code MoH CR is CZ/CA01. 2) Používejte kódy států podle ISO 3166: (1993), např.: 2) Please use the codes for the different countries acc. to ISO 3166 (1993), e.g.: AT ... Rakousko/Austria BE ... Belgie/Belgium CH ... Švýcarsko/Switzerland CZ ... Česká republika/Czech Republic DE ... Německo/Germany DK ... Dánsko/Denmark ES ... Španělsko/Spain FI ... Finsko/Finland FR ... Francie/France GB ... Velká Británie/United Kingdom GR ... Řecko/Greece IE ... Irsko/Ireland IS ... Island/Iceland IT ... Itálie/Italy LI ... Lichtenštejnsko/Liechtenstein LU ... Lucembursko/Luxembourg NL ... Nizozemí/Netherlands NO ... Norsko/Norway PT ... Portugalsko/Portugal SE ... Švédsko/Sweden SK ... Slovensko/Slovakia 3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999, částka 33/1999 Sb. 3) Please use the district codes prescribed by CSO Disposition from 27.4.1999, part 33/1999 Coll. 4) Rok, měsíc, den (v položce 1200 vyplňuje Ministerstvo zdravotnictví) 4) Year, month, day (column 1200 is filled in by Ministery of Health) 5) Bude vydáno příslušným úřadem. Skládá se z dvoumístného kódu státu podle ISO 3166, lomítka a kódu příslušného úřadu, lomítka a vnitřního registračního čísla určeného úřadem: např.: CZ/CA01/nnn... 5) To be assigned by the competent authority. Composed of the two-letter country code of ISO 3166 followed by a slash, the code of the competent authority, a slash and an internal registration number, e.g.: CZ/CA01/nnn... 6) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení změny". Uvádějí se pouze změny, které nemění zařazení zdravotnických prostředků do klasifikační třídy, do skupiny zdravotnických prostředků nebo jeho účel použití (tj. položky 1500, 1510, 1580, 1581, 1582). V opačném případě je nutno provést registraci nového zdravotnického prostředku. Při "Hlášení změny" nebo "Odvolání změny" musí být uvedeno "Dřívější registrační číslo". Uvádějí se pouze změněné položky a u položek, které se vypouštějí bez náhrady se uvede text "vypustit". 6) In each notificaton of change the box "notification of change" must be marked. This notification concerns only changes in which the classification class, group of medical device or the intended use of the medical device (items 1500, 1510, 1580, 1581, 1582) is not changed. If any of these items is changed, it is necessary to register a new medical device and terminate the previous registration. Only the changed items are filled in; in items which should be deleted fill in the text "vypustit". For each "Notification of change" or "Withdrawal of notification" the "previous registration number" must be filled in. 7) Výroba zahrnuje i montáž, balení, manipulaci, sterilizaci, obnovu, označování zdravotnického prostředku a určení účelu jeho použití. 7) Manufacturing also covers e.g. assembling, packaging, processing, sterilizing, refurbishing, labeling and specifying the intended purpose of the medical device. 8) Vyplní výrobce nebo jeho zplnomocněný zástupce. Skládá se z dvoumístného kódu státu (ISO 3166), lomítka a identifikačního (IČO) čísla výrobce nebo jeho zplnomocněného zástupce. 8) Assigned by the manufacturer or the representative. This code is always composed of the two-letter country code of ISO 3166 followed by a slash and the identity-number of manufacturer/representative. 9) Vyplnit jestliže výrobce nemá sídlo v ČR. 9) To be filled in if the manufacturer is not located in the CZ. 10) Uveďte patřičný kód a název skupiny zdravotnického prostředku podle Univerzálního nomenklaturního systému zdravotnických prostředků (UMDNS) (např. 10966; obvazy, mul). Není-li k dispozici, prosím uveďte krátký popis (č. 1500...). 10) Please enter the relevant code and its designation from the nomenclature Universal Medical Device Nomenclature System (UMDNS) (e.g. 10966; Compresses, Gauze). If not available, please give a short description (No. 1500...). 11) Kód a název kategorie jsou založeny na ČSN EN ISO 15225. Prostředek se označuje kódem první vhodné kategorie, do které spadá v pořadí od písmene a do písmene l. 11) Device category code and term are based on ČSN EN ISO 15225:2000. The device should be assigned to the first category in which it fits, moving from a to l. +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |Kód | | |Code| | | |kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R| | | | |cat.| | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g| | |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h| | |Active implantable devices | | |Electro mechanical medical devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i| | |Non-active implantable devices | | |opakované použití | | | | | | |Reusable instruments | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j| | |Dental devices | | |Single use devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k| | |prostředky | | |Technical aids for disabled persons | | | |Ophthalmic and optical devices | | | | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l| | |a terapii zářením | | |Hospital hardware | | | |Diagnostic and therapeutic radiation | | | | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ 12) Povinné jen pokud nebyl uveden kód a název skupiny zdravotnického prostředku. Zvolte sami vhodný stručný (heslovitý) popis. Může obsahovat základní vlastnosti prostředku, jako např. předpokládané použití, hlavní aspekty klasifikace, sterilní, metrologické vlastnosti, vztah k obsaženému léku atd. 12) Only compulsory, if no relevant code/designation has been given. Please use appropriate terms or a short phrase. It can include basic features of the product such as, for example, the intended use, the aspects governing its classification, sterile, metrological qualities, the relationship to an incorporated drug, the principal mode of action ... 13) Je možné uvést více položek. 13) Multiple entries possible. 14) Použijte zvláštní list, jestliže je to zapotřebí. 14) Use additional sheet if necessary. Příl.XXI Formulář hlášení o klinických zkouškách Clinical Investigation Notification Form



Obec ........................ Datum ..................... City Date Jméno, příjmení ..................... Podpis a razítko........... Name, long Signature Poznámky a jiná sdělení:/Notes and other information:7)
Pokyny k vyplnění Formuláře hlášení o klinickém zkoušení podle zákona č. 123/2000 Sb., o zdravotnických prostředcích a o změně některých souvisejících zákonů. Notes on completing the Clinical Investigation Notification Form according to Medical Devices Act No. 123/2000 Coll. 1) Kód je složen z dvoumístného označení státu podle ISO 3166, lomítka, písmen CA a čísla příslušného úřadu v daném státě, např.: kód MZ je CZ/CA01. 1) Composed of the two-letter country code of ISO 3166 followed by a slash, CA and the number of the competent authority in the state, e.g.: CZ/CA01. 2) Používejte prosím kódy států podle ISO 3166, např.: 2) Please use the codes for the different countries acc. to ISO 3166 (1993), e.g.: AT ... Rakousko/Austria BE ... Belgie/Belgium CH ... Švýcarsko/Switzerland CZ ... Česká republika/Czech Republic DE ... Německo/Germany DK ... Dánsko/Denmark ES ... Španělsko/Spain FI ... Finsko/Finland FR ... Francie/France GB ... Velká Británie/United Kingdom GR ... Řecko/Greece IE ... Irsko/Ireland IS ... Island/Iceland IT ... Itálie/Italy LI ... Lichtenštejnsko/Liechtenstein LU ... Lucembursko/Luxembourg NL ... Nizozemí/Netherlands NO ... Norsko/Norway PT ... Portugalsko/Portugal SE ... Švédsko/Sweden SK ... Slovensko/Slovakia 3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999, částka 33/1999 Sb. 3) Please use the district codes prescribed by CSO Disposition from 27.4.1999, part 33/1999 Coll. 4) Bude vydáno příslušným úřadem. Skládá se z kódu státu podle ISO 3166, lomítka a kódu příslušného úřadu, lomítka a vnitřního registračního čísla určeného úřadem: např.: CZ/CA01/nnn... 4) To be assigned by the competent authority. Composed of the two-letter country code of ISO 3166 followed by a slash, the code of the competent authority, a slash and an internal registration number, e.g.: CZ/CA01/nnn... 5) Vyplní výrobce nebo zplnomocněný zástupce. Kód je složen z dvoumístného označení státu podle ISO 3166, lomítka a identifikačního čísla (IČO) výrobce nebo zplnomocněného zástupce. 5) Assigned by the manufacturer/authorized representative. This code is always composed of the two-letter country code of ISO 3166 followed by a slash and the identity-number of manufacturer/authorized representative. 6) Rok, měsíc, den 6) Year, month, day 7) Použijte další list papíru, jestliže je to třeba. Uveďte všechna zúčastněná zdravotnická zařízení včetně jejich adresy (město, stát). 7) Use additional sheet if necessary. 8) Vyplňte správný kód a název skupiny zdravotnického prostředku podle Univerzálního nomenklaturního systému zdravotnických prostředků (UMDNS) (např. 16516, kardiostimulátory, vnější neinvazivní). Pokud není k dispozici, uveďte prosím stručný popis (číslo kolonky 4760). 8) Please enter the relevant code and its designation from the nomenclature Universal Medical Device Nomenclature System (UMDNS) (e.g. 16516; Pacemakers, Cardiac, External Noninvasive). If not available, please give a short description (No. 4760). 9) Kód a název kategorie jsou založeny na normě ČSN EN ISO 15225. Zdravotnický prostředek se označuje kódem první vhodné kategorie, do které spadá v pořadí od písmene a do písmene l. 9) Device category code and term are based on ČSN EN ISO 15225:2000. The device should be assigned to the first category in which it fits, moving from a to l. +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |Kód | | |Code| | | |kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R| | | | |cat.| | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g| | |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h| | |Active implantable devices | | |Electro mechanical medical devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i| | |Non-active implantable devices | | |opakované použití | | | | | | |Reusable instruments | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j| | |Dental devices | | |Single use devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k| | |prostředky | | |Technical aids for disabled persons | | | |Ophthalmic and optical devices | | | | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l| | |a terapii zářením | | |Hospital hardware | | | |Diagnostic and therapeutic radiation | | | | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ 10) Označte důležité informace pro identifikaci zkoušeného zdravotnického prostředku. 10) Please indicate the necessary data for the identification of the medical device to be tested. Příl.XXII Formulář pro registraci informací vztahujících se k certifikaci zdravotnických prostředků Form for the registration of information relating to the certification of medical devices



Prohlašuji, že uvedené informace jsou podle mého vědomí a svědomí správné. I affirm that the information given above is correct to the best of my knowledge. Obec ........................ Datum ..................... City Date Jméno, příjmení ..................... Podpis a razítko........... Name, long Signature Poznámky a jiná sdělení:/Notes and other information:10)
Pokyny k vyplnění formuláře povinného hlášení podle § 31 zákona č. 123/2000 Sb. Notes on completing the General Obligation to Notify Form according to § 31 Medical Devices Act No. 123/2000 Coll. 1) Kód příslušného úřadu se skládá z dvoumístného kódu státu podle ISO 3166, lomítka, písmen CA a čísla příslušného úřadu v daném státě, například: kód MZ je CZ/CA01. 1) Composed of the two-letter country code of ISO 3166 followed by a slash, CA and the number of the competent authority in the state, e.g.: code MoH CR is CZ/CA01. 2) Používejte kódy států podle ISO 3166: 2) Please use the codes for the different countries acc. to ISO 3166 (1993), e.g.: AT ... Rakousko/Austria BE ... Belgie/Belgium CH ... Švýcarsko/Switzerland CZ ... Česká republika/Czech Republic DE ... Německo/Germany DK ... Dánsko/Denmark ES ... Španělsko/Spain FI ... Finsko/Finland FR ... Francie/France GB ... Velká Británie/United Kingdom GR ... Řecko/Greece IE ... Irsko/Ireland IS ... Island/Iceland IT ... Itálie/Italy LI ... Lichtenštejnsko/Liechtenstein LU ... Lucembursko/Luxembourg NL ... Nizozemí/Netherlands NO ... Norsko/Norway PT ... Portugalsko/Portugal SE ... Švédsko/Sweden SK ... Slovensko/Slovakia 3) Používejte kódy okresů podle Opatření ČSÚ ze dne 27.4.1999, částka 33/1999 Sb. 3) Please use the district codes prescribed by CSO Disposition from 27.4.1999, part 33/1999 Coll. 4) Rok, měsíc, den 4) Year, month, day 5) Při každém hlášení změny je nutno zaškrtnout značku "Hlášení změny". Uvádějí se pouze změny, které nemění zařazení zdravotnických prostředků do klasifikační třídy, do skupiny zdravotnické prostředky nebo jeho určený účel použití tj. položky 5320, 5620, 5630). V opačném případě je nutno provést registraci nového zdravotnického prostředku. Uvádějí se pouze změněné položky a u položek, které se vypouštějí bez náhrady se uvede text "vypustit". Při "Hlášení změny" musí být uvedeno "Dřívější registrační číslo". 5) In each notificaton of change the box "notification of change" must be marked. This notification concerns only changes in which the classification class, group of medical device or the intended use of the medical device (items 5320, 5620, 5630) is not changed. If any of these items is changed, it is necessary to register a new medical device and terminate the previous registration. Only the changed items are filled in; in items which should be deleted fill in the text "vypustit". Each "Notification of change" the "previous registration number" must be filled in. 6) Vydání, odvolání, pozastavení, odmítnutí a ukončení se vztahují k certifikátu; změny a doplnění se vztahují k certifikaci zdravotnického prostředku. Seznam zdravotnických prostředků je možno rozšířit nebo modifikovat v rozsahu certifikátu systému úplného zabezpečení jakosti. 6) Issued, withdrawn, suspended, refused and terminated is certificate-related. Modified and complemented is product-related. Under a given certificate for a full quality assurance system, the list of products can be enlarged (complemented) or products may be modified. 7) Toto číslo je vydáno příslušnou autorizovanou osobou. 7) This number is issued by the Notified Body involved. 8) Certifikát má být vydán autorizovanou osobou pro každou schválenou šarži (resp. pro každý jednotlivý zdravotnický prostředek). Pro informaci poskytovanou v rámci výměny dat mezi výrobcem a autorizovanou osobou postačuje najít v databázi druh certifikátu vydaného výrobci pro daný zdravotnický prostředek a identifikovat (kódem) autorizované osoby, která jej vydala. 8) For EC verification, the directives require the Notified Bodies to issue a certificate for each batch (or for each individual product) which is accepted. For the information provided in the context of the regulatory data exchange by a given Notified Body, it is sufficient to find in the data base the kind of certificate which has been granted to the manufactuer of a given device and the identity of the Notified Body which issued it. 9) To se vztahuje i k orgánům posuzujícím shodu v souladu s dohodami o vzájemném uznávání certifikace mezi EU a dalšími státy. 9) This also applies accordingly to conformity assessment bodies designated in the Mutual Recognition Agreements. 10) V případě potřeby použijte další listy. 10) Use additional sheet if necessary. 11) Vyplní výrobce nebo zplnomocněný zástupce. Skládá se z dvoumístného kódu státu podle ISO 3166, lomítka a identifikačního (IČO) čísla výrobce nebo zplnomocněného zástupce. 11) Assigned by the manufacturer or the representative. This code is always composed of the two-letter country code of ISO 3166 followed by a slash and the identity-number of manufacturer/representative. 12) Vyplnit pokud výrobce není v ČR. 12) To be filled in if the manufacturer is not located in the CZ. 13) Určitý výrobní model nebo varianta modelu podle specifikace uvedené v certifikátu. Údaj povinný pro certifikáty podle bodu 4 přílohy II nebo podle přílohy III nebo podle přílohy IV, nepovinný pro ostatní certifikáty. 13) Specific manufacturer model or family model as specified in the certificate. Mandatory for a certificate issued against point 4 of annex 2/II or against annex 3/III or against annex 4/IV; optional for other certificates. 14) Uvádějte označení a kód podle Univerzálního nomenklaturního systému zdravotnických prostředků (UMDNS). Pozor: Udejte jen jedno označení pro jeden zdravotnický prostředek (např. 16516 stimulátory, srdeční, vnější neinvasivní). Pokud není k dispozici, udejte prosím stručný popis (č. 5620...). Pro každý další zdravotnický prostředek použijte zvláštní kopii této stránky. 14) Generic device group code and term have to be taken from ECRI Universal Medical Device Nomenclature System (UMDNS). Please note: Only one generic device code/term should be taken for one medical device (e.g. 16516; Pacemakers, Cardiac, External Noninvasive). If not available, please give a short description (No. 5620...). Please use for each additional medical device a separate copy of this page. 15) Kód a název kategorie jsou založeny na normě ČSN EN ISO 15225. Výrobek se označuje kódem první vhodné kategorie, do které spadá v pořadí od písmene a do písmene l. 15) Device category code and term are based on CSN EN ISO 15225:2000. The device should be assigned to the first category in which it fits, moving from a to l. +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |Kód | | |Code| | | |kat.|Název kategorie zdrav. prostředků |P|of |Name of category of medical devices |R| | | | |cat.| | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |06 |Diagnostické zdravotnické prostředky in vitro |a| 02 |Anestetické a respirační zdravotnické prostředky|g| | |In vitro diagnostic devices | | |Anaesthetic/respiratory devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |01 |Aktivní implantabilní zdravotnické prostředky |b| 04 |Elektro/mechanické zdravotnické prostředky |h| | |Active implantable devices | | |Electro mechanical medical devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |07 |Neaktivní implantabilní zdravotnické prostředky|c| 09 |Zdravotnické prostředky - nástroje pro |i| | |Non-active implantable devices | | |opakované použití | | | | | | |Reusable instruments | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |03 |Stomatologické zdravotnické prostředky |d| 10 |Zdravotnické prostředky pro jednorázové použití |j| | |Dental devices | | |Single use devices | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |08 |Oftalmologické a optické zdravotnické |e| 11 |Zdravotnické prostředky pro postižené osoby |k| | |prostředky | | |Technical aids for disabled persons | | | |Ophthalmic and optical devices | | | | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ |12 |Zdravotnické prostředky pro diagnostiku |f| 05 |Zdravotnické prostředky v nemocničním vybavení |l| | |a terapii zářením | | |Hospital hardware | | | |Diagnostic and therapeutic radiation | | | | | +----+-----------------------------------------------+-+----+------------------------------------------------+-+ 16) Povinné jen v případě, že nebylo udáno označení a kód. Uveďte vlastní označení nebo stručnou větu. Ta může zahrnovat hlavní rysy zdravotnického prostředku, např. předpokládané použití, významné aspekty pro jeho klasifikaci, sterilní nebo měřicí vlastnosti, vztah k obsaženým léčivům ... 16) Only compulsory, if no relevant code/designation has been given. Please use appropriate terms or a short phrase. The phrase can include basic features of the product such as, for example, the intended use, the aspects governing its classification, the sterile or metrological qualitfication, the relationship with an incorporated drug, the principal means of action ...